Tin tức
Giá trị của các dấu ấn sinh học trong sàng lọc, chẩn đoán, đánh giá hiệu quả điều trị và tiên lượng ung thư dạ dày
- 23/06/2020 | Giá trị của xét nghiệm IgE đặc hiệu dị nguyên trong chẩn đoán bệnh dị ứng
- 17/05/2020 | Giá trị xét nghiệm Creatinin máu bao nhiêu là mắc bệnh suy thận
- 27/07/2020 | Giá trị của kháng nguyên liên quan đến lõi của virus viêm gan B (HBcrAg)
- 15/04/2020 | Giá trị chẩn đoán của các xét nghiệm phân tử và kháng thể ở bệnh nhân bị COVID-19
- 01/10/2020 | Giá trị của các dấu ấn sinh học trong chẩn đoán, theo dõi và tiên lượng ung thư biểu mô tế b...
Tóm tắt
1) Ung thư dạ dày là một nhóm các loại khối u đa dạng về sinh học và di truyền học; có nhiều yếu tố khác nhau trong nguyên nhân của ung thư, gồm các yếu tố môi trường và di truyền. Hầu hết các trường hợp ung thư dạ dày (90-95%) là ung thư thể tuyến.
2) Ung thư dạ dày là một loại khối u ác tính với tỷ lệ mắc và tử vong cao trên toàn cầu. Mặc dù nội soi và chẩn đoán hình ảnh đã cải thiện sự phát hiện các tổn thương liên quan đến ung thư biểu mô dạ dày giai đoạn đầu, ung thư dạ dày có các hình thái không đồng nhất về hình thái.
3) Mức độ pepsinogen I với giá trị cắt ≤70 ng/mL và tỷ lệ PGI/II với giá trị cắt ≤3,0 có thể được sử dụng trong sàng lọc và chẩn đoán sớm viêm teo và ung thư dạ dày với độ nhạy và độ đặc hiệu ở mức độ trung bình.
4) Giá trị tham chiếu bình thường của CEA, CA 19-9 và CA 72-4 tương ứng là 0-6,5 ng/mL, 0-37 U/ mL và 0-5,7 U/mL. Nồng độ huyết thanh trước phẫu thuật cao của CA19-9 và CA72-4 có liên quan đến nguy cơ tử vong cao hơn, nồng độ CEA trước hóa trị liệu cao (>50 ng/mL) có thể giúp dự đoán sự tiến triển của bệnh sau hóa trị liệu và sự giảm của CA72 -4 (>70%) có thể giúp dự đoán đáp ứng của bệnh đối với hóa trị liệu.
5) Gần đây, một số dấu ấn sinh học đã trở thành mục tiêu phân tử cho các liệu pháp điều trị ung thư dạ dày, bao gồm sự sinh mạch, thụ thể của yếu tố tăng trưởng biểu bì 2 (HER2), sự chuyển tiếp biểu mô-trung mô (MET), thụ thể của yếu tố tăng trưởng biểu bì (EGFR), đích của rapamycin ở động vật có vú (mTOR), sự chết được lập trình-1 (PD-1), DNA, ... 5 thuốc điều trị đích đã được FDA phê chuẩn cho bệnh ung thư dạ dày tiến triển, gồm trastuzumab, ramucirumab, penbrolizumab, telatinib và masitinib.
*
The value of biomarkers in screening, diagnosis, assessment of therapy efficacy and prognostic prediction of gastric cancer
Luat Nghiem Nguyen
MEDLATEC General Hospital
Abstract
1) Gastric cancer is a group of tumor types which are diverse in their biology and genetics; there are various factors at work in the etiology of the cancer, including environmental and genetic factors. Most cases of stomach cancers (90-95%) are adenocarcinomas.
2) Gastric cancer is a malignant tumor type with high rates of incidence and mortality globally. Although endoscopy and imaging technology have improved the detection of early-stage gastric carcinoma-associated lesions, gastric cancer has a wide range of morphological heterogeneity.
3) Pepsinogen I level with cut-off value of ≤70 ng/mL and PGI/II ratio with cut-off value ≤3.0 may be used in screening and early diagnosis of atrophic gastritis and gastric cancer with medium levels of sensitivity and specificity.
4) Normal reference values for CEA, CA 19-9 and CA 72-4 and CEA were assumed to be 0-6.5ng/mL, 0-37 U/mL, and 0-5.7 U/mL respectively. The high preoperative serum levels of CA19-9 and CA72-4 are associated with higher risk of death, high pretreatment CEA levels (>50 ng/mL) may predict clinical disease progression after chemotherapy, and a decrease (>70%) of CA72-4 may predict pathologic response to chemotherapy.
5) Recently, some biomarkers has become the molecular targets for targeted therapies of gastric cancer, including the angiogenesis, human epidermal growth factor receptor 2 (HER2), mesenchymal-epithelial transition (MET), epidermal growth factor receptor (EGFR), mammalian target of rapamycin (mTOR), programmed death-1 (PD-1) and DNA, ... Five targeted therapy drugs have been approved by FDA for advanced gastric cancer, including trastuzumab, ramucirumab, penbrolizumab, telatinib and masitinib.
*
Theo GLOBOCAN, thuộc Tổ chức Y tế thế giới (WHO), trong năm 2018, số ung thư dạ dày mới đối với cả hai giới được phát hiện trên thế giới là 1.033.701 ca, chiếm 5,7% tổng số ung thư, đứng thứ 6 sau ung thư phổi, vú đại trực tràng và thuyến tiền liệt, nhưng đứng thứ 3 về số ca tử vong do ung thư trên toàn thế giới, với 782.685 ca tử vong, chiếm 8,2%, sau ung thư phổi và ung thư đại trực tràng (Bray F, 2018 [1]).
Ở Việt Nam, cũng theo GLOBOCAN, trong năm 2018, số ung thư dạ dày mới đối với cả hai giới là 17.527 ca, chiếm 10,6% tổng số ung thư, sau ung thư gan và phổi, đứng thứ 3 về ung thư ở nam giới với 11.161 ca, chiếm 12,3%, sau ung thư gan và phổi, và đứng thứ 4 ở nữ với 6.366 ca, chiếm 8,6%, sau ung thư vú, đại trực tràng và phổi. Số ca tử vong do ung thư dạ dày ở Việt Nam 2018 là 15.065 ca, đứng hàng thứ 3 sau ung thư gan và phổi.
Ung thư dạ dày là một bệnh đa yếu tố bởi vì nhiều yếu tố di truyền và môi trường đóng vai trò trong sinh ung thư, bao gồm cả cơ sở di truyền của vật chủ, tác nhân nhiễm khuẩn như Helicobacter pylori (H. pylori), Epstein-Barr virus (EBV) và lối sống (uống rượu, hút thuốc lá và chế độ ăn uống). Do không có các triệu chứng đặc hiệu, ung thư dạ dày thường bị chẩn đoán nhầm hoặc chẩn đoán muộn. Phẫu thuật, hóa trị liệu và xạ trị là các phương pháp điều trị ung thư dạ dày phổ biến nhất. Tiên lượng ung thư dạ dày là kém, tỷ lệ sống sót sau 5 năm là dưới 25% và tỷ lệ sống trung bình chỉ là 7 đến 10 tháng sau khi được chẩn đoán.
Mục đích của bài tổng quan này là nhằm cung cấp một cái nhìn tổng quan về giá trị của các dấu ấn sinh học cổ điển và các dấu ấn sinh học phân tử mới trong sàng lọc, chẩn đoán, đánh giá hiệu quả điều trị và tiên lượng ung thư dạ dày.
1. Giá trị của các dấu ấn sinh học cổ điển trong chẩn đoán ung thư dạ dày
Các dấu hiệu khối u cổ điển thường được sử dụng trong chẩn đoán ung thư dạ dày là pepsinogen I (PGI), tỷ số PGI/II, kháng nguyên carcinoembryonic (CEA), kháng nguyên carbohydrate 19-9 (CA 19-9) và kháng nguyên carbohydrate 72-4 (CA 72-4). Ngoài ra, hai dấu ấn khối u kháng nguyên carbohydrate CA125 (CA125) và alpha-fetoprotein (AFP) đôi khi cũng được sử dụng để đánh giá nguy cơ di căn của một vài loại ung thư dạ dày.
1.1. Giá trị của pepsinogen I và tỷ lệ PG I/II trong sàng lọc ung thư dạ dày
Pepsinogen (PG) là tiền enzym (proenzyme) của pepsin - một enzym thủy phân protein- được bài tiết bởi các tế bào niêm mạc của dạ dày. Pepsinogen là một protein gồm 375 gốc acid amin, có khối lượng phân tử 42 kDa. Pepsinogen tồn tại dưới hai dạng: pepsinogen I (PG I) và pepsinogen II (PG II). Pepsinogen I được tổng hợp bởi các tế bào chính của niêm mạc ở vùng đáy dạ dày, trong khi PG II được tổng hợp bới các tế bào niêm mạc của toàn bộ các vùng của dạ dày và của hành tá tràng (Hình 1).
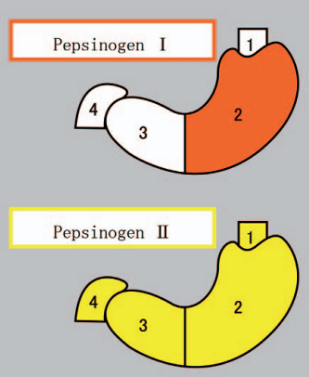
Hình 1. Sự sản xuất pepsinogen I (màu đỏ) và pepsinogen 2 (màu vàng) ở các vùng khác nhau của dạ dày và hành tá tràng: 1) vùng tâm vị (cardia), 2) vùng đáy vị (fundus), 3) vùng hang môn vị (pylonic antrum), 4) hành tá tràng (duodenum).
Mức độ PGI huyết thanh với giá trị cắt (cut-off) ≤ 70 ng/mL và tỷ lệ PGI/II với giá trị cắt là ≤3,0 được xem là giá trị (+) tính đối với tiền ung thư (precancerous diseases of stomach) và ung thư dạ dày. Đối với ung thư dạ dày, quá trình tổn thương về bệnh học tế bào diễn biến theo các giai đoạn: viêm dạ dày mạn (chronic gastritis), viêm teo dạ dày mạn (atrophic chronic gastritis), dị sản (metaplasia) và loạn sản (dysplasia).
1.1.1. Giá trị của PGI, PGII và tỷ số PGI/PGII trong chẩn đoán viêm teo dạ dày
Trong viêm teo dạ dày (atrophic gastritis), mức độ PGI và tỷ lệ PG I/ II huyết thanh ở bệnh nhân viêm teo dạ dày giảm một cách rất rõ rệt so với người khỏe mạnh (Bảng 1).
Bảng 1. Mức độ PGI, PGII và tỷ số PGI/PGII huyết tương ở bệnh nhân viêm teo dạ dày (De Re, 2016) [3]).
![Bảng 1. Mức độ PGI, PGII và tỷ số PGI/PGII huyết tương ở bệnh nhân viêm teo dạ dày (De Re, 2016) [3]).](/ImagePath/images/20201017/20201017_dau-an-ung-thu-da-day.png)
Ở bệnh nhân viêm teo dạ dày có H. pylori (-) tính và (+) tính, mức độ PGI, PGII và tỷ số PGI/PGII có sự khác nhau một cách có ý nghĩa rõ rệt (Bảng 2), vì vậy, khi đánh giá kết quả sàng lọc viêm teo dạ dày cần chú ý điều này. Mức độ của PGI, PGII và tỷ số PGI/PGII ở bệnh nhân viêm teo dạ dày có H. pylori (-) tính và (+) tính được thể hiện ở Bảng 2.
Bảng 2. Mức độ của PGI, PGII và tỷ số PGI/PGII ở bệnh nhân viêm teo dạ dày có H. pylori (-) tính và (+) tính (Dinis-Ribeiro M, 2004) [4]).
![Bảng 2. Mức độ của PGI, PGII và tỷ số PGI/PGII ở bệnh nhân viêm teo dạ dày có H. pylori (-) tính và (+) tính (Dinis-Ribeiro M, 2004) [4]).](/ImagePath/images/20201017/20201017_dau-an-ung-thu-da-day-1.png)
1.1.2. Giá trị của PGI, PGII và tỷ số PGI/PGII trong chẩn đoán loạn sản và ung thư dạ dày giai đoạn sớm
Nghiên cứu nồng độ pepsinogen I, II và tỷ số PGI/II huyết thanh trên 186 bệnh nhân quá sản dạ dày mức độ thấp (low grade dysplasia), quá sản dạ dày mức độ cao (high grade dysplasia) và ung thư dạ dàygiai đoạn sớm (early gastric cancer), Cha JH và Jang JS, 2018 [2] thu được kết quả như được chỉ ra ở Bảng 3.
Bảng 3. Nồng độ pepsinogen I, pepsinogen II và tỷ số PGI/II huyết thanh trong loạn sản và ung thư dạ dày giai đoạn sớm (Cha JH và Jang JS, 2018 [2])
|
Dấu ấn khối u |
Tổng số (n = 186) |
Loạn sản mức độ thấp (n=82) |
Loạn sản mức độ cao (n=37) |
Ung thư dạ dàygiai đoạn sớm (n=67) |
P |
|
PGI (ng/mL) |
55,1 ± 44,1 |
50,1 ± 43,4 |
50,4 ± 42,2 |
63,8 ± 45,3 |
0,132 |
|
PGII (ng/mL) |
18,1 ± 12,8 |
17,9 ± 13,6 |
17,0 ± 12,5 |
19,1 ± 12,0 |
0,715 |
|
Tỷ số PGI/II |
3,2 ± 1,8 |
2,9 ± 1,7 |
3,2 ± 1,6 |
3,7 ± 1,8 |
0,015 |
Tổng kết 19 nghiên cứu trên tổng số 169.009 ca ung thư dạ dày, Liu L, 2019 [6] thấy rằng giá trị của pepsinogen I và tỷ số PGI/II để phát hiện sớm ung thư dạ dày chỉ ở mức trung bình, tương ứng với độ nhạy là 56% (53%-59%), độ đặc hiệu là 71% (70%-71%) và độ chính xác (ROC) là 56% (45%-68%). Vì vậy, khi nghi ngờ, cần chỉ định nội soi dạ dày.
1.2. Giá trị của CEA, CA19-9 và CA72-4 trong chẩn đoán ung thư dạ dày
Các dấu ấn sinh học cổ điển có thể được sử dụng trong chẩn đoán, theo dõi hiệu quả điều trị, đánh giá tái phát và tiên lượng ung thư dạ dày gồm CEA, CA19-9 và CA72-4. Tỷ lệ dương tính của các dấu ấn khối u CEA, CA19-9 và CA72-4 một mình, kết hợp bộ đôi hay bộ ba trong ung thư dạ dày được thể hiện ở Bảng 4.
Bảng 4. Tỷ lệ dương tính trước điều trị của các dấu ấn khối u trong ung thư dạ dày (Sun Z, 2019 [9])
![Bảng 4. Tỷ lệ dương tính trước điều trị của các dấu ấn khối u trong ung thư dạ dày (Sun Z, 2019 [9])](/ImagePath/images/20201017/20201017_dau-an-ung-thu-da-day-3.png)
Về giá trị của các dấu ấn khối u CEA, CA19-9 và CA72-4 trong đánh giá sự tiến triển của ung thư dạ dày, ở giai đoạn bệnh càng nặng, tỷ lệ dương tính của các dấu ấn khối u càng cao, tuy nhiên, cho dù ở giai đoạn nặng nhất (giai đoạn IV), tỷ lệ dương tính của các dấu ấn khối u này cũng không vượt quá 50% số ca (Hình 2).
![Hình 2. Tỷ lệ % dương tính của các dấu ấn khối u ở các giai đoạn ung thư dạ dày (Shimada H, 2014 [8]).](/ImagePath/images/20201017/20201017_hinh-2.png)
Hình 2. Tỷ lệ % dương tính của các dấu ấn khối u ở các giai đoạn ung thư dạ dày (Shimada H, 2014 [8]).
1.3. Giá trị của CEA, CA19-9, CA72-4 trong đánh giá hiệu quả điều trị ung thư dạ dày
Giá trị của các dấu ấn khối u CEA, CA19-9, CA72-4 trong đánh giá hiệu quả của điều trị ung thư dạ dày trước và sau hóa trị liệu được thể hiện ở Bảng 5.
Bảng 5. Mức độ của các dấu ấn khối u CEA, CA19-9 và CA72-4 trước và sau hóa trị liệu (Sun Z, 2019 [9]).
![Bảng 4. Mức độ của các dấu ấn khối u CEA, CA19-9 và CA72-4 trước và sau hóa trị liệu (Sun Z, 2019 [9]).](/ImagePath/images/20201017/20201017_dau-an-ung-thu-da-day-4.png)
Kết quả cho thấy trong số các dấu ấn khối u CEA, CA19-9 và CA72-4, chỉ có CEA và CA72-4 có giá trị trong đánh giá hiệu quả của điều trị ung thư dạ dày.
1.4. Giá trị của CEA, CA19-9, CA72-4 trong đánh giá nguy cơ tái phát ung thư dạ dày
Để đánh giá nguy cơ tái phát (risk of recurrence) ung thư dạ dày sau phẫu thuật, các dấu ấn khối u phải được định lượng trong vòng 2 tuần trước khi bệnh nhân được phẫu thuật, sử dụng các giá trị cắt (cut-off) của CEA là 5 ng/mL, của CA19-9 là 36 U/mL và của CA72-4 là 4 U/mL. Nguy cơ tái phát được tính theo số điểm (scores) của tỷ lệ tăng mức độ của các dấu ấn khối u so với giá trị cắt của các dấu ấn khối u (tumor marker cut-off ratio: TMR). Số điểm được chia thành bốn loại (0, 1, 2 và 3 trở lên). Nguy cơ tái phát ung thư dạ dày sau điều trị trong 5 năm (60 tháng) được đánh giá bằng số điểm cho các mức điểm 0, 1, 2 và 3 trở lên, tương ứng là 12,8%, 23,9%, 45,5% và 68,3% (P<0,05) (Hình 3).
![Hình 3. Nguy cơ tái phát ung thư dạ dàytheo thời gian (tháng) được đánh giá bằng số điểm (score) so với giá trị cắt của các dấu ấn khối u (TMR) (Lee JC, 2013 [5]).](/ImagePath/images/20201017/20201017_dau-an-ung-thu-da-day-6.png)
Hình 3. Nguy cơ tái phát ung thư dạ dàytheo thời gian (tháng) được đánh giá bằng số điểm (score) so với giá trị cắt của các dấu ấn khối u (TMR) (Lee JC, 2013 [5]).
1.5. Giá trị của CEA, CA19-9, CA72-4 trong tiên lượng ung thư dạ dày
Trong số các dấu ấn sinh học CEA, CA19-9 và CA72-4, chỉ có CA19-9 và CA72-4 huyết thanh trước trị liệu có giá trị đánh giá tiên lượng (tỷ lệ sống sót: survival) của bệnh nhân theo thời gian. Tỷ lệ sống sót % của bệnh nhân (theo tháng) được đánh giá theo mức độ CA19-9 (< và ≥80 U/mL) và CA72-4 (< và ≥20 U/mL) trước trị liệu được thể hiện ở Hình 4.
![Hình 4. Tỷ lệ sống sót của bệnh nhân trị liệu trước trị liệu theo mức độ CA19-9 và CA72-4. (A) Tỷ lệ sống sót chung ở những bệnh nhân có CA19-9 ≥80 U/mL thấp hơn so với những bệnh nhân có CA19-9 <80 U/mL (8,4 so với 15,0 tháng, P=0,023). (B) Tỷ lệ sống sót chung của bệnh nhân có CA72-4 ≥20 U/mL cũng thấp hơn so với những bệnh nhân có CA72-4 <20 U/mL (9,9 so với 16,3 tháng, P = 0,006) (Sun Z, 2019 [9]).](/ImagePath/images/20201017/20201017_dau-an-ung-thu.png)
Hình 4. Tỷ lệ sống sót của bệnh nhân trị liệu trước trị liệu theo mức độ CA19-9 và CA72-4. (A) Tỷ lệ sống sót chung ở những bệnh nhân có CA19-9 ≥80 U/mL thấp hơn so với những bệnh nhân có CA19-9 <80 U/mL (8,4 so với 15,0 tháng, P=0,023). (B) Tỷ lệ sống sót chung của bệnh nhân có CA72-4 ≥20 U/mL cũng thấp hơn so với những bệnh nhân có CA72-4 <20 U/mL (9,9 so với 16,3 tháng, P = 0,006) (Sun Z, 2019 [9]).
2. Giá trị của các dấu ấn phân tử mới trong chẩn đoán ung thư dạ dày
Các thuốc hóa trị liệu thường được sử dụng như 5-fluorouracil (5-FU), fluoropyrimidine, bạch kim, taxan, irinotecan và anthracycline, có tác dụng tiêu diệt tế bào ung thư, nhưng cũng độc với các tế bào lành của cơ thể. Gần đây, sự phát triển của các thuốc nhắm đích phân tử (molecular targeted agents), có tác dụng ức chế các con đường tín hiệu gây ung thư, đã thúc đẩy việc cá thể hóa (personalized) trong chẩn đoán, điều trị và cải thiện đáng kể kết quả điều trị ung thư dạ dày.
2.1. Vai trò của các dấu ấn phân tử mới trong ung thư dạ dày
Cho đến nay, nhiều dấu ấn sinh học mới của ung thư dạ dày đang được nghiên cứu và bắt đầu được sử dụng có thể có vai trò trong chẩn đoán, phân lớp phân tử (molecular subtypes), điều trị đích (targeted therapy) và liệu pháp miễn dịch (immunotherapy). Vai trò của các dấu ấn sinh học trong điều trị đích ung thư dạ dày được tóm tắt ở Bảng 6.
Bảng 6. Vai trò của các dấu ấn sinh học trong ung thư dạ dày (Ye DM, 2020 [11])
|
Dấu ấn sinh học |
Vai trò chung |
Vai trò cụ thể |
Các dấu ấn sinh học |
|
Các dấu ấn sinh học ung thư dạ dày |
Dự đoán |
Sử dụng chung |
Pepsinogen I, PGI/II, CEA, CA19-9, CA72-4 |
|
Nguy cơ cao |
MG7-Ag, PG, G-17, HP |
||
|
Chẩn đoán |
Ung thư biểu mô (Adenocarcinoma) |
CDX-2, CD10, MUC2, … |
|
|
Các type đặc biệt |
AFP, EBV, E-cadherin, |
||
|
LNM (Lymph node micrometastasis): vi di căn hạch lympho |
CK, KAM5-2, CD31, D2-40 |
||
|
Phân lớp phân tử |
UNG THƯ DẠ DÀY (The cancer genome Atlas): bản đồ bộ gen ung thư |
EBV, MSI, GS, CIN |
|
|
ACRG (Asian Cancer Research Group): nhóm nghiên cứu ung thư Châu Á |
MSI, MSS/EMT, MSS/TP53+, MSS/P53 |
||
|
Điều trị |
Hóa trị liệu (Chemotherapy) |
Ki67 (thấp -> nguy cơ tái phát) |
|
|
Điều trị đích (Targeted therapy) |
HER-2, VEGF2, EGFR, C-MET, Claudia 18-2 (quá mức) |
||
|
Điều trị miễn dịch (Immunotherapy) |
PD-1/PD-L1 (đột biến), dMMR/MSI-H, EBV, … |
||
|
Các vai trò trò khác |
Methyl hóa DNA |
hMLH1, CDH1, .. (quá mức) |
|
|
NcRNA (RNA không mã hóa) |
miRNAs, IncRNA, circRNA |
||
|
Chu trình tế bào (Cell cycle) |
P27, P53, P16, … (đột biến) |
||
|
Sự chết tế bào được lập trình (Apoptosis) |
Bcl-2 (thể hiên giảm) |
||
|
Tiên lượng (Prognosis) |
CD133, CD44 (quá mức) |
Ghi chú: CD (cluster of differentiation): cụm biệt hóa; MUC2: mucin 2; AFP: α-fetoprotein; EBV (Epstein Barr virus); HER-2 (human epidermal growth factor receptor 2): thụ thể của yếu tố tăng trưởng biểu mô 2; erb-b2 thụ thể tyrosine kinase 2; VEGFR2 (vascular endothelial growth factor receptor 2): thụ thể của yếu tố tăng trưởng nội mô mạch máu 2; EGFR (epidermal growth factor receptor): thụ thể của yếu tố tăng trưởng biểu bì; PD-1 (programmed cell death 1): sự chết tế bào được lập trình 1; dMMR (deficient mismatch repair): sửa lỗi ghép cặp không đầy đủ; MSI-H (high levels of microsatellite instability): mức độ không ổn định cao của vi vệ tinh; hMLH1 (human mutL homolog 1): gen sửa chữa bắt cặp sai của người 1; CDH1(cadherin-1): protein xuyên màng type 1 phụ thuộc ion calci; miRNAs: các microRNA; lncRNA (long non-coding RNA): RNA không mã hóa dài; CircRNA (circular RNA): RNA vòng.
2.2. Giá trị của các dấu ấn phân tử mới trong định hướng điều trị đích ung thư dạ dày
Các con đường tín hiệu, sự biểu hiện của các dấu ấn sinh học mới, cơ chế tác động của các thuốc kháng thể đơn dòng (monoclonal antibodies) và thuốc phân tử nhỏ (small molecules) trong điều trị đích ung thư dạ dày được thể hiện ở Hình 5.
![Hình 5. Sơ đồ các con đường tín hiệu, sự biểu hiện của các dấu ấn sinh học mới, cơ chế tác động của các thuốc kháng thể đơn dòng và các thuốc phân tử nhỏ trong điều trị đích ung thư dạ dày (Wadhwa R, 2013 [10]).](/ImagePath/images/20201017/20201017_dau-an-ung-thu-1.png)
Hình 5. Sơ đồ các con đường tín hiệu, sự biểu hiện của các dấu ấn sinh học mới, cơ chế tác động của các thuốc kháng thể đơn dòng và các thuốc phân tử nhỏ trong điều trị đích ung thư dạ dày (Wadhwa R, 2013 [10]).
Giá trị của các dấu ấn phân tử mới trong các thử nghiệm pha III đã kết thúc với các thuốc điều trị đích trong ung thư dạ dày tiến triển được thể hiện ở Bảng 7.
Bảng 7. Giá trị của các dấu ấn phân tử mới trong các thử nghiệm pha III đã kết thúc với các thuốc điều trị đích trong ung thư dạ dày tiến triển (Selim JH, 2019 [7]).
|
Dấu ấn đích |
Thuốc điều trị đích |
Thử nghiệm |
Dấu ấn đích/Thiết kế thử nghiệm |
Lợi ích sống sót/tháng, điều trị so với đối chứng |
|---|---|---|---|---|
|
HER2 |
Trastuzumab |
ToGA/dòng 1 |
HER2/hóa trị liệu với trastuzumab hoặc không |
Có (HR 0,74)/13,8 so với 11,1 |
|
Trastuzumab |
HELOISE/ dòng 1 pha IIIb |
HER2/hóa trị liệu so với trastuzumab liều cao |
Không (HR 1,24)/12,5 so với 10,6 |
|
|
Trastuzumab/pertuzumab |
JACOB/dòng 1 |
HER2/trastuzumab với hóa trị liệu, pertuzumab hoặc giả dược |
Không (HR 0,84)/17,5 so với 14,2 |
|
|
Trastuzumab emtansine (T-DM1) |
GATSBY/ dòng 2 |
HER2/T-DM1 so với taxane |
Không (HR 1,15)/7,9 so với 8,6 |
|
|
Lapatinib |
LoGIC/ dòng 1 |
HER2/hóa trị liệu với lapatinib hoặc giả dược |
Không (HR 0,91)/12,2 so với 10,5 |
|
|
Lapatinib |
Tytan/ dòng 2 |
HER2/paclitaxel với hoặc không có lapatinib |
Không (HR 0,84)/11,0 so với 8,9 |
|
|
Sự tạo thành mạch máu (Angiogenesis) |
Bevacizumab |
AVAGAST/ dòng 1 |
Không/hóa trị liệu với bevacizumab hoặc giả dược |
Không (HR 0,87)/12,1 so với 10,1 |
|
Bevacizumab |
AVATAR/ dòng 1 |
Không/hóa trị liệu với bevacizumab hoặc giả dược |
Không (HR 1,11)/10,5 so với 11,4 |
|
|
Ramucirumab |
RAINFALL/ dòng 1 |
HER2(−)/hóa trị liệu với ramucirumab hoặc giả dược |
Không (HR 0,96)/11,2 so với 10,7 |
|
|
Ramucirumab |
RAINBOW/ dòng 2 |
Không/paclitaxel với ramucirumab hoặc giả dược |
Có (HR 0,807)/9,6 so với 7,4 |
|
|
Ramucirumab |
REGARD/ dòng 2 và 3 |
Không/ramucirumab so với giả dược |
Có (HR 0,776)/5,2 so với 3,8 |
|
|
Apatinib |
NCT01512745/dòng 3 |
Không/apatinib so với giả dược |
Có (HR 0,71)/6,5 so với 4,7 |
|
|
PD-1/PD-L1 |
Nivolumab |
ATTRACTION2/dòng 3 |
Không/nivolumab so với giả dược ở các bệnh nhân Châu Á |
Có (HR 0,63)/5,26 so với 4,14 |
|
Pembrolizumab |
KEYNOTE-061/dòng 2 |
PD-L1/pembrolizumab so với paclitaxel |
Không (HR 0,82)/9,1 so với 8,3 |
|
|
Pembrolizumab |
KEYNOTE-181/ dòng 2 |
PD-L1/pembrolizumab so với hóa trị liệu |
Có (HR 0,69)/9,3 so với 6,7 trong PD-L1 ≥ 10% |
|
|
Pembrolizumab |
KEYNOTE-062/ dòng 1 |
PD-L1 & HER2 (-) /pembrolizumab hoặc pembrolizumab với hóa trị liệu so với đơn hóa trị liệu |
Không, pembrolizumab/hóa trị liệu (HR 0,91)/10,6 so với 11,1. Không, pembrolizumab với hóa trị liệu/hóa trị liệu (HR 0,85)/12,5 so với 11,1 |
|
|
Avelumab |
JAVELIN Gastric 300/dòng 3 |
Không/avelumab so với hóa trị liệu |
Không (HR 1,1)/4,6 so với 5,0 |
|
|
DNA |
TAS-102 |
TAGS/ dòng 3 |
Không/TAS-102 so với giả dược |
Có (HR 0,69)/5,7 so với 3,6 |
|
EGFR |
Cetuximab |
EXPVÀ/ dòng 1 |
Không/hóa trị liệu có hoặc không cetuximab |
Không (HR 1,03)/9,4 so với 10,7 |
|
Panitumumab |
REAL3/ dòng 1 |
Không /hóa trị liệu có hoặc không panitumumab |
Không (HR 1,37)/8,8 so với 11,3 |
|
|
STAT3 |
Napabucasin |
BRIGHTER/ dòng 2 |
Không /paclitaxel với napabucasin hoặc giả dược |
Không (HR 1,01)/6,93 so với 7,36 |
|
PARP |
Olaparib |
GOLD/dòng 2 |
Không /paclitaxel với olaparib hoặc giả dược |
Không (HR 0,79 [97,5% CI 0,63-1,00])/8,8 so với 6,9 |
|
MMP-9 |
Andecaliximab |
GAMMA-1/dòng 1 |
HER2(-)/mFOLFOX6 có ecaliximab hoặc giả dược |
Không (HR 0,93)/12,5 so với 11,8 |
|
MET |
Onartuzumab |
METGastric/ dòng 1 |
MET và HER2(-)/mFOLFOX6 với onartuzumab hoặc giả dược |
Không (HR 0,82)/11,0 so với 11,3 |
|
Rilotumumab |
RILOMET-1/dòng 1 |
MET và HER2(-)/hóa trị liệu với rilotumumab |
Không (HR 1,34)/8,8 so với 10,7 |
|
|
mTOR |
Everolimus |
GRANITE-1/dòng 3) |
Không /everolimus so với giả dược |
Không (HR 0,90)/5,4 so với 4,3 |
Ghi chú: HER2 (human epidermal growth factor receptor 2): thụ thể của yếu tố tăng trưởng biểu bì 2 của người; angiogenesis (sự tạo mạch máu mới); HR (hazard ratio): tỷ lệ nguy cơ, PD-1 (programmed death-1): sự chết được lập trình-1; PD-L1 (programmed death ligand 1): phối tử của sự chết được lập trình-1; DNA: deoxyribonucleic acid; EGFR (epidermal growth factor receptor): thụ thể yếu tố tăng trưởng biểu bì; STAT3 (signal transducer and activator of transcription 3): bộ chuyển đổi tín hiệu STAT3 và bộ kích hoạt của sự phiên mã 3; PARP: poly (ADP-ribose) polymerase; MMP-9 (matrix metalloproteinase 9): metallicoproteinase-9 của của chất khuôn; mFOLFOX6 (5-fluorouracil/leucovorin/oxaliplatin); MET (mesenchymal-epithelial transition): sự chuyển tiếp biểu mô - trung mô; mTOR (mammalian target of rapamycin): đích của rapamycin ở động vật có vú.
Các thuốc kháng thể đơn dòng và các thuốc phân tử nhỏ với các dấu ấn sinh học phân tử mới tương ứng được sử dụng cho điều trị đích ung thư dạ dày đã được FDA phê chuẩn, được thể hiện ở Bảng 8.
Bảng 8. Các thuốc kháng thể đơn dòng và các thuốc phân tử nhỏ với các dấu ấn sinh học phân tử mới tương ứng được sử dụng cho điều trị đích ung thư dạ dày đã được FDA phê chuẩn (Selim JH, 2019 [7]; Ye DM, 2020 [11]).
|
Loại thuốc |
Thuốc |
Phân tử đích |
Cơ chế tác dụng |
FDA phê chuẩn |
|
Kháng thể đơn dòng (monoclonal antibodies) |
Trastuzumab |
HER2 |
Gắn với HER2, ngăn chặn sự phát triển, tăng sinh và sự sống sót của tế bào ung thư. |
2010 |
|
Ramucirumab |
VEGFR2 |
Ngăn chặn sự kích hoạt VEGFR-2, ức chế sự hình thành mạch máu. |
2014 |
|
|
Penbrolizumab |
PD-1 |
Gắn với thụ thể PD-1, ngăn chặn tương tác PD-L1 và PD-L2, giải phóng ức chế miễn dịch, tăng đáp ứng miễn dịch chống khối u. |
2017 |
|
|
Thuốc phân tử nhỏ (small molecules) |
Telatinib |
VEGF |
Ức chế chọn lọc thụ thể VEGFR, PDGFR và Kit tyrosine kinases, ức chế sự hình thành mạch máu. |
2011 |
|
Masitinib |
PK |
Ức chế c-Kit tyrosine kinase, ức chế sự hoạt hóa ung thư phụ thuộc cKit và cảm ứng sự chết được lập trình (apotosis). |
2015 |
Ghi chú: HER2 (human epidermal growth factor receptor 2): thụ thể của yếu tố tăng trưởng biểu bì 2 của người; VEGFR2 (vascular endothelial growth factor receptor 2): thụ thể của yếu tố tăng trưởng nội mô mạch máu 2; PD-1 (programmed death-1): sự chết được lập trình-1; PD-L1 (programmed death ligand 1): phối tử của sự chết được lập trình-1; EGFR (epidermal growth factor receptor): thụ thể yếu tố tăng trưởng biểu bì; PK: tyrosine kinase.
Ngoài các dấu ấn sinh học phân tử mới đã hoàn thành thử nghiệm lâm sàng pha III nêu trên, nhiều dấu ấn sinh học phân tử mới trong điều trị đích đang được thử nghiệm lâm sàng pha I và II (Selim JH, 2019 [7]; Ye DM, 2020 [11]).
Gần đây, khi nghiên cứu bộ protein (proteomics) huyết tương, phân tích bằng phổ khối - sắc ký lỏng (liquid chromatography-tandem mass spectrometry: LC-MS/MS) kết hợp với ghi dấu các phân tử sinh học (tandem mass tags labeling), Zhou B và cộng sự, 2020 [12] đã phát hiện 2040 protein khác nhau, trong đó 11 protein có sự khác biệt về nồng độ có ý nghĩa ở bệnh nhân ung thư dạ dày giai đoạn sớm so với những đối chứng khỏe mạnh. Các nghiên cứu về bộ protein huyết tương nhằm phát hiện sớm ung thư dạ dày hiện đang được tiếp tục.
Tài liệu tham khảo
1. Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2018; 68: 394-424. (Necula L, 2019)
2. Cha JH, Jamg JS. Clinical correlation between serum pepsinogen level and gastric atrophy in gastric neoplasm. Korean J Intern Med 2018 Nov 07; 35(3): 550-558.
3. De Re V, Orzes E, Canzonieri V, et al. Pepsinogens to Distinguish Patients With Gastric Intestinal Metaplasia and Helicobacter pylori Infection Among Populations at Risk for Gastric Cancer. Clin Transl Gastroentr 2016; 7: e183.
4. Dinis-Ribeiro M, da Costa-pereira A, Lopes C. Validity of Serum Pepsinogen I/II Ratio for the Diagnosis of Gastric Epithelial Dysplasia and Intestinal Metaplasia during the Follow-Up of Patients at Risk for Intestinal-Type Gastric Adenocarcinoma. Neoplasia 2004 Sep; 6(5): 449-456.
5. Lee JC, Lee SY, Kim CY, and Yang DH. Clinical utility of tumor marker cutoff ratio and a combination scoring system of preoperative carcinoembryonic antigen, carbohydrate antigen 19-9, carbohydrate antigen 72-4 levels in gastric cancer. J Korean Surg Soc 2013 Dec; 85(6): 283-289.
6. Liu L, Lang J, Jin YL, et al. The Value of Pepsinogen in GC Screening: A Systematic Review and Meta-Analysis. Gastroenterol Res Pract 2019 Jan 21; 2019: 1-11.
7. Selim JH, Shaheen S, Sheu WC, and Hsueh CT. Targeted and novel therapy in advanced gastric cancer. Exp Hematol Oncol 2019 Oct 11; 8: 25.
8. Shimada H, Noie T, Ohashi M, Oba K, Takahashi Y. Clinical significance of serum tumor markers for gastric cancer: a systematic review of literature by the Task Force of the Japanese Gastric Cancer Association. Gastric cancer 2014; 17: 26-33.
9. Sun Z, Jia J, Du F, et al. Clinical significance of serum tumor markers for advanced gastric cancer with the first-line chemotherapy. Transl Cancer Res 2019; 8(8): 2680-2690.
10. Wadhwa R, Song S, Lee JS, et al. Gastric Cancer: Molecular and Clinical Dimensions. Nat Rev Clin Oncol 2013 Nov; 10(11): 643-655.
11. Ye DM, Xu G, Ma W, et al. Significant function and research progress of biomarkers in gastric cancer. Oncol Lett 2020; 19(1): 17-29.
12. Zhou B, Zhou Z, Chen Y, et al. Plasma proteomics-based identification of novel biomarkers in early gastric cancer. Clinical Biochemistry 2020 Feb; 76: 5-10.
Bình luận ()
Lựa chọn dịch vụ
Quý khách hàng vui lòng lựa chọn dịch vụ y tế theo nhu cầu!