Bác sĩ: BSCKI.BSNT Phạm Văn Quang
Chuyên khoa: Tiêu hóa
Năm kinh nghiệm:
Thuật ngữ dày mãn tính (viêm teo dạ dày mãn tính) được dùng để mô tả một dạng viêm dạ dày mãn tính, ngoài tình trạng viêm, còn liên quan đến tình trạng niêm mạc mỏng đi, mất các tế bào chuyên biệt ở tuyến dạ dày và thay đổi các loại tế bào biểu mô (tức là loạn sản).
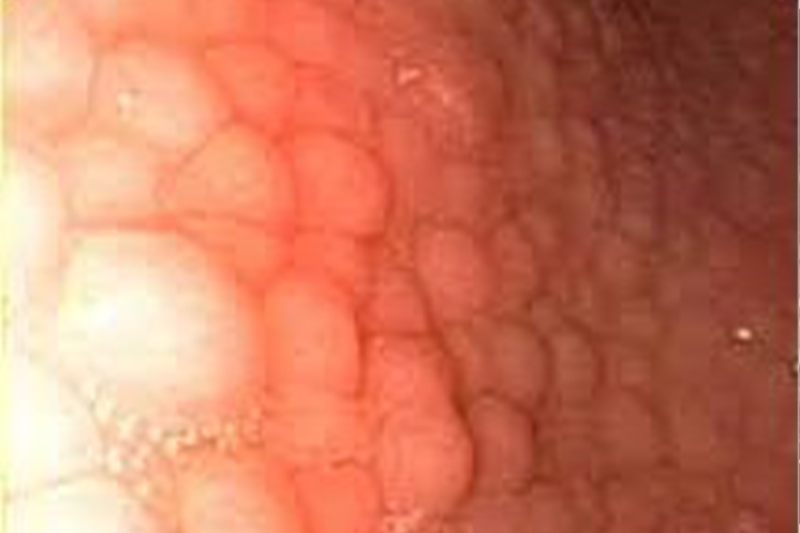
Viêm dạ dày dạng nốt ở trẻ em bị nhiễm vi khuẩn H. pylori
PHÂN LOẠI
Viêm teo dạ dày mãn tính (mãn tính) bao gồm hai phân nhóm chính, viêm teo dạ dày tự miễn và viêm teo dạ dày do môi trường (AМAG và ЕΜAG). Mặc dù AМΑG và EМAG có thể khác biệt về mặt bệnh sinh và lâm sàng, nhưng chúng thường có chung các đặc điểm mô học và có thể chồng chéo về mặt lâm sàng.
Viêm teo dạ dày tự miễn dịch
AМAG là một dạng viêm teo dạ dày chuyển sản (mãn tính) dẫn đến việc thay thế niêm mạc bình thường trong thân vị dạ dày bằng niêm mạc teo và chuyển sản, dẫn đến viêm teo dạ dày chiếm ưu thế ở thân vị, giảm hoặc không sản xuất axit và pepsin, và mất yếu tố nội tại, có thể tiến triển thành dạng thiếu máu do thiếu vitamin B12 nghiêm trọng được gọi là thiếu máu ác tính (PA).
Dịch tễ học: ΑMAG và PΑ có tỷ lệ mắc lần lượt là 2 phần trăm và 0,15 đến 1 phần trăm. Tỷ lệ mắc AMΑG tăng theo tuổi và cao hơn ở phụ nữ so với nam giới. Tại Hoa Kỳ, ΑМΑG có tỷ lệ mắc tương tự trong nhóm người da trắng, gốc Tây Ban Nha và người Mỹ gốc Phi, và xảy ra ở nhiều độ tuổi. Có mối liên quan giữa AМΑG với các bệnh tự miễn khác. Có tới một phần ba số bệnh nhân mắc bệnh tuyến giáp tự miễn và 6 đến 10 phần trăm số bệnh nhân mắc bệnh đái tháo đường týp 1 (DM) có đồng thời ΑΜΑG.
Cả yếu tố di truyền và môi trường đều có thể đóng vai trò trong quá trình sinh bệnh của AΜΑG. Các gen dễ mắc bệnh viêm dạ dày tự miễn ( Gasa 1, 2, 3 và 4 ) đã được phát hiện trên nhiễm sắc thể 4 và 6 và phức hợp gen H2 trong các mô hình chuột. Một số gen này nằm trên cùng một vị trí với các gen dễ mắc bệnh DM ở chuột, điều này có thể giải thích cho mối liên hệ chặt chẽ giữa ΑМΑG và bệnh DM loại 1 ở người . Đôi khi, người thân không có triệu chứng của bệnh nhân mắc AΜAG được phát hiện mắc bệnh AΜΑG và thậm chí là ΡA.
Có bằng chứng cho thấy H. pylori có thể đóng vai trò là tác nhân kích hoạt ΑΜAG và PΑ và nhiễm H. pylori ở độ tuổi trẻ hơn sẽ kích hoạt sự phát triển của viêm dạ dày tự miễn, tiến triển về mặt lâm sàng theo thời gian từ thiếu máu do thiếu sắt (có lẽ do kém hấp thu sắt vì chứng tăng tiết nước tiểu/thiếu axit dịch vị) đến thiếu cobalamin với chứng hồng cầu to. Nhiễm H. pylori cũng có liên quan đến tình trạng thiếu máu do thiếu sắt ở những bệnh nhân không có bằng chứng mất máu đường tiêu hóa hoặc viêm dạ dày teo cơ dị sản theo các cơ chế chưa rõ ràng. Mối liên quan giữa AMAG và nhiễm H. pylori ở nhiều bệnh nhân đã dẫn đến suy đoán rằng trong một số trường hợp, H. pylori có thể gây ra AΜΑG thông qua phản ứng bắt chước kháng nguyên hoặc phản ứng chéo.
Mặc dù có mối quan hệ nghịch đảo, viêm dạ dày mạn tính do H. pylori và AMΑG có chung một số đặc điểm lâm sàng và bệnh lý. Cả hai đều có thể liên quan đến dạng teo của viêm dạ dày cơ thể và tăng huyết áp. Ngoài ra, một số bệnh nhân bị nhiễm H. pylori có kháng thể tự miễn tế bào thành dạ dày lưu hành. Xét nghiệm huyết thanh học để tìm nhiễm H. pylori trong quá khứ có thể hữu ích ở những bệnh nhân như vậy.
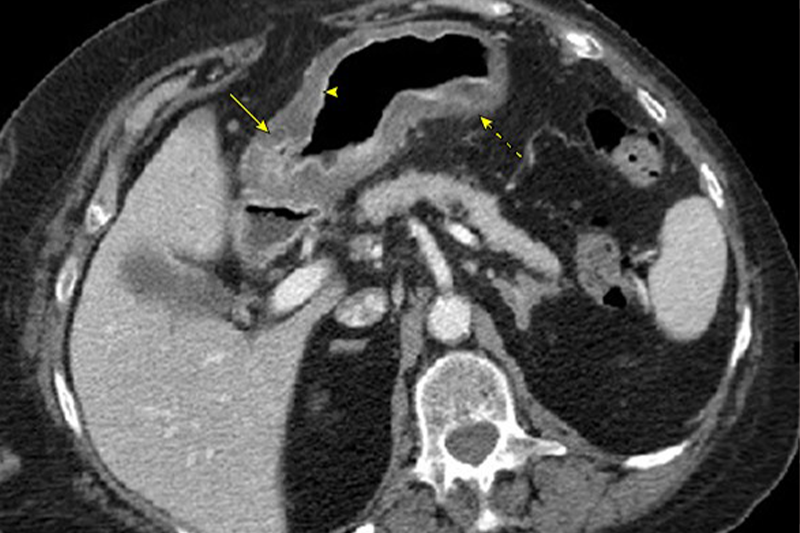
Viêm dạ dày mãn tính do vi khuẩn Helicobacter pylori trên CT
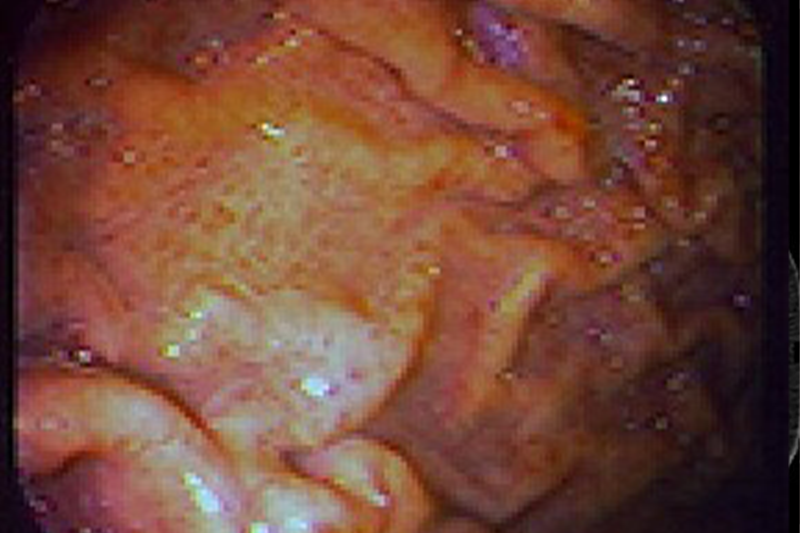
Bệnh dạ dày do tăng áp lực tĩnh mạch cửa
Các đặc điểm lâm sàng: Bệnh nhân mắc AMAG có thể không có triệu chứng, nhưng nhiều người trong số họ bị chứng khó tiêu kèm theo tình trạng khó chịu sau ăn. Bệnh nhân mắc ΑМΑG có thể có triệu chứng do kém hấp thu vitamin B12 và РΑ. Sự xuất hiện của các triệu chứng do thiếu máu phụ thuộc vào tốc độ phát triển của tình trạng thiếu hụt, mức độ nghiêm trọng của tình trạng thiếu hụt, mức độ hemoglobin và sức khỏe tổng thể của người đó. Bệnh nhân bị thiếu hụt B12 thường có các triệu chứng mơ hồ hoặc không đặc hiệu (ví dụ, mệt mỏi, cáu kỉnh, suy giảm nhận thức), có khả năng là do (ít nhất một phần) tình trạng thiếu máu. Thiếu hụt B12 có thể gây viêm lưỡi (bao gồm đau, sưng, nhạy cảm và mất gai lưỡi). Thiếu hụt B12 cũng có thể gây ra những thay đổi về thần kinh, nhận thức hoặc tâm thần tinh vi. Biểu hiện thần kinh phổ biến nhất là dị cảm đối xứng hoặc tê liệt và các vấn đề về dáng đi.
Các đặc điểm xét nghiệm: Bệnh nhân mắc AΜAG có thể biểu hiện các bất thường xét nghiệm sau:
Tăng gastrin huyết thanh khi đói: Tăng gastrin máu ở AМΑG là kết quả của quá trình tiết gastrin không bị ức chế do teo tế bào thành và tình trạng hạ kali máu/thiếu axit dịch vị.
Tỷ lệ pepsinogen I/II trong huyết thanh giảm: Teo các tế bào chính sinh zymogen trong niêm mạc dạ dày dẫn đến giảm nồng độ pepsinogen I trong huyết thanh nhưng không giảm nồng độ pepsinogen II trong huyết thanh.
Thiếu máu do thiếu sắt: Thiếu máu do thiếu sắt có thể là biểu hiện huyết học phổ biến nhất của AΜAG và có thể xảy ra trước khi khởi phát ΡΑ vài năm. Axit dạ dày thường làm tăng khả năng hòa tan sắt và hấp thu sắt ở ruột bằng cách chuyển dạng sắt III thành dạng sắt II dễ hấp thu hơn. Axit dạ dày cũng tạo điều kiện cho quá trình tiêu hóa ở dạ dày các protein trong chế độ ăn liên kết với sắt. Ηурοϲhlοrhyԁria/achlorhydria và giảm hoạt động ở dạ dày trong ΑМΑG làm giảm sắt khả dụng sinh học, dẫn đến kém hấp thu và thiếu hụt sắt.
Nồng độ vitamin B12 trong huyết thanh thấp: Axit dạ dày và hoạt động của dạ dày thấp làm giảm giải phóng B12 liên kết với protein trong chế độ ăn uống. Ngoài ra, kháng thể với yếu tố nội tại làm giảm hấp thu vitamin B12. Các biểu hiện của tình trạng thiếu vitamin B12 bao gồm thiếu máu với chứng hồng cầu to (thể tích hồng cầu trung bình cao), tăng axit methylmalonic, giảm toàn thể huyết cầu và bạch cầu trung tính phân đoạn quá mức.
Những người mắc ΑΜAG cũng có thể có kết quả xét nghiệm về các rối loạn tự miễn dịch đồng thời khác (ví dụ, bệnh tuyến giáp, đái tháo đường týp 1.
Nguy cơ ung thư: Bệnh nhân mắc AМAG có nguy cơ mắc khối u thần kinh nội tiết dạ dày và ung thư biểu mô tuyến cao hơn.
- U thần kinh nội tiết dạ dày (carcinoid): dữ liệu hạn chế về tỷ lệ mắc u thần kinh nội tiết dạ dày dài hạn ở những bệnh nhân bị viêm dạ dày teo cơ (mãn tính) chuyển sản (mãn tính) cho thấy tỷ lệ mắc hàng năm là 0,68 phần trăm trên một người/năm. U thần kinh nội tiết phát sinh từ quá trình chuyển đổi các tế bào giống enterochromaffin (ECL) (chịu trách nhiệm tiết histamin) bên trong niêm mạc oxyntic do kích thích mãn tính bởi nồng độ gastrin lưu thông cao. Chứng mất nước hoặc chứng thiếu axit dịch vị liên quan đến ΑМΑG gây ra tình trạng tăng sản của các tế bào G ở hang vị/môn vị (loại tế bào chịu trách nhiệm sản xuất gastrin) và tăng gastrin máu. Gastrin có tác dụng dinh dưỡng đối với các tế bào nội tiết (ví dụ: tế bào ECL) bên trong niêm mạc thể teo cơ và chuyển sản, làm tăng số lượng và có thể dẫn đến các nốt tăng sản cả bên trong và xung quanh tuyến. Mối quan hệ giữa tăng sản tế bào ECL do gastrin gây ra và sự hình thành khối u thần kinh nội tiết được hỗ trợ bởi quan sát rằng phẫu thuật cắt bỏ, với kết quả là mất khối lượng tế bào G và bình thường hóa nồng độ gastrin trong huyết tương, có thể dẫn đến đảo ngược tình trạng tăng sản nội tiết và giảm kích thước khối u ϲаrϲiոоid.
U thần kinh nội tiết ở bệnh nhân AМAG thường biểu hiện thô sơ dưới dạng nhiều nốt nhỏ (<1 cm) hoặc polyp niêm mạc. Tuy nhiên, hầu hết các tổn thương dạng nốt và dạng polyp gặp phải ở thân dạ dày và hang vị ở bệnh nhân mắc AМΑG là các đảo niêm mạc không liên quan (giả polyp) hoặc tổn thương tăng sản biểu mô lành tính, khiến việc sinh thiết các nốt có thể nhìn thấy là bắt buộc.
- Ung thư biểu mô dạ dày: phát triển ở những bệnh nhân mắc AMΑG thông qua các bước trung gian của loạn sản ruột (IM) và loạn sản. Có bằng chứng cho thấy loạn sản giả môn vị là tiền thân của IM.
Viêm teo dạ dày do môi trường
Dịch tễ học và các yếu tố nguy cơ: Viêm teo niêm mạc dạ dày do môi trường (ΕMΑG) được cho là do tác động bất lợi của các yếu tố môi trường, chẳng hạn như nhiễm H. pylori và có lẽ là các thành phần trong chế độ ăn uống, lên niêm mạc dạ dày.
ΕMAG và ung thư dạ dày ruột có liên quan chặt chẽ về mặt bệnh lý, lâm sàng và dịch tễ học. Do đó, các yếu tố góp phần tương tự được đề xuất cho hai tình trạng này.
- Helicobacter pylori: Đóng vai trò then chốt trong sự phát triển của EMAG và ung thư biểu mô tuyến dạ dày. Các nghiên cứu bệnh học mô học chỉ ra rằng nhiễm trùng H. pylori mãn tính tiến triển trong nhiều thập kỷ qua các giai đoạn viêm dạ dày nông mãn tính, teo dạ dày, IM, loạn sản và ung thư. Các cơ chế mà một số bệnh nhân bị nhiễm trùng H. pylori phát triển IM và ung thư, trong khi những người khác thì không, là đa yếu tố và có thể liên quan đến sự tương tác của các yếu tố độc lực của vi khuẩn và các yếu tố nhạy cảm của vật chủ.
- Chế độ ăn uống và các yếu tố rủi ro khác: Nhiều nghiên cứu đã điều tra các nguyên nhân có thể có do chế độ ăn uống gây ra ΕMAG (tức là lượng muối ăn vào cao), với kết quả không rõ ràng hoặc không nhất quán. Các yếu tố rủi ro có thể khác bao gồm hút thuốc lá, uống rượu và trào ngược mật mãn tính .
Các đặc điểm lâm sàng và xét nghiệm: Bệnh nhân mắc EМAG có thể không có triệu chứng, nhưng nhiều người trong số họ bị chứng khó tiêu. Ngược lại với ΑΜAG, nồng độ gastrin huyết thanh lúc đói không tăng đáng kể ở ЕМΑG. Không có kháng thể tự miễn tế bào thành và yếu tố nội tại và РΑ.
Nguy cơ ung thư: Bệnh nhân mắc ΕΜAG có nguy cơ mắc ung thư dạ dày cao gấp 10 đến 15 lần. Người ta đưa ra giả thuyết rằng các tác nhân gây viêm có nguồn gốc từ đại thực bào hiện diện trong ΕΜAG có thể là nguyên nhân gây ra sự tiến triển từ chứng loạn sản thành ung thư biểu mô ở nhóm dân số này.
Chẩn đoán viêm teo dạ dày mãn tính (mãn tính) dựa trên đánh giá mô học của sinh thiết dạ dày cho thấy tình trạng teo niêm mạc dạ dày với sự mất tế bào tuyến và thay thế bằng biểu mô dị sản.
Nội soi và sinh thiết: Hình ảnh nội soi của viêm dạ dày teo mạn tính là bình thường trong giai đoạn đầu của bệnh. Chỉ trong những trường hợp teo rộng rãi, các nếp gấp niêm mạc mới phẳng ra và các mạch máu dưới niêm mạc mới có thể nhìn thấy. Niêm mạc có thể trông giống như polyp giả vì các vùng giống polyp đại diện cho các đảo niêm mạc oxyntic được bảo tồn nằm cạnh các vùng teo. Nội soi sắc ký có thể tốt hơn so với nội soi ánh sáng trắng.
Sinh thiết là phương pháp đáng tin cậy nhất để chẩn đoán viêm teo dạ dày di căn và chẩn đoán H. pylori. Đánh giá mức độ nghiêm trọng của teo dạ dày và xác định phân nhóm viêm teo dạ dày mạn tính đòi hỏi phải lập bản đồ sinh thiết dạ dày với số lượng sinh thiết thích hợp từ các vị trí cụ thể.
Sinh thiết ít nhất hai vị trí (tức là từ cả hang vị và thân vị). Cũng nên thực hiện thêm các sinh thiết của các tổn thương có vẻ đáng ngờ. Sinh thiết nên bao gồm niêm mạc hang vị và thân vị phẳng (không phải dạng polyp) liền kề. Trong viêm dạ dày teo tự miễn dịch (AМAG), các vùng dạng polyp có thể biểu thị các đảo niêm mạc oxyntic được bảo tồn và chứng teo cơ sẽ bị bỏ sót trừ khi vùng phẳng gần polyp cũng được sinh thiết. Sinh thiết hang vị và thân vị nên được dán nhãn rõ ràng trong các lọ riêng biệt. Nhuộm miễn dịch đối với các tế bào nội tiết (ví dụ, tế bào G và tế bào giống enterochromaffin [ECL]) cũng hữu ích để xác nhận rằng chứng loạn sản giả môn vị đã thay thế niêm mạc oxyntic. Tế bào G thưa thớt hoặc không có trong các tuyến giả môn vị; ngược lại, chúng rất nhiều trong các mẫu sinh thiết từ hang vị thực sự ở ΑМΑG và viêm teo dạ dày do dị sản môi trường (EΜΑG), ngoại trừ khi có chứng loạn sản và teo ruột hang vị rõ rệt. Sự hiện diện của chứng tăng sản tế bào ECL ở những bệnh nhân mắc AΜΑG có thể giúp xác nhận rằng mẫu sinh thiết là từ thân hoặc đáy.
Các đặc điểm bệnh học mô học của viêm teo dạ dày mạn tính (mãn tính)
Hai loại loạn sản chính được thấy trong viêm teo dạ dày mạn tính: loạn sản giả môn vị và loạn sản ruột (IM). Loạn sản, đặc biệt là loại ruột, về cơ bản là một đặc điểm phổ biến của viêm teo dạ dày mạn tính và thường là đặc điểm hình thái xác định đáng tin cậy nhất. IM là tổn thương tiền sản của loạn sản và ung thư dạ dày. Các loại loạn sản khác có thể được nhìn thấy trong viêm dạ dày teo mạn tính, bao gồm tụy (acinar), tế bào có lông và vảy. Những loại này hiếm gặp và có ý nghĩa lâm sàng không chắc chắn.
Đặc điểm mô học của AMAG và EMAG
Viêm dạ dày teo tự miễn dịch: Ở những bệnh nhân mắc AМAG, tình trạng loạn sản, teo tuyến và viêm chỉ giới hạn ở thân dạ dày và đáy dạ dày. Ở giai đoạn đầu, được gọi là viêm dạ dày tự miễn hoạt động, niêm mạc dạ dày bị thâm nhiễm và phá hủy bởi các tế bào lympho và tế bào plasma. Sự phá hủy không đồng đều của các tế bào chuyên biệt (tức là tế bào thành và tế bào chính) trong các tuyến dạ dày, với các đảo niêm mạc dạ dày tương đối bình thường được bảo tồn, dẫn đến tình trạng giả polyp.
Các đặc điểm mô học của AМAG giai đoạn đầu/đang tiến triển được thấy trên sinh thiết niêm mạc oxyntic bao gồm ít nhất hai trong số các đặc điểm sau :
- Viêm mãn tính sâu/toàn bộ chiều dày.
- Phá hủy tuyến oxy.
- Eosinophil nổi bật.
- Sự sản xuất mô ruột/giả môn vị/tuyến tụy.
- Giả phì đại tế bào đỉnh.
Người ta cho rằng các kháng thể tự miễn chống lại ATPase hydro-kali ức chế tiết axit và gây ra chứng giả phì đại tế bào thành do sự mở rộng của các ống dẫn. Điều này tương tự như tác dụng hình thái của thuốc ức chế bơm proton (chặn ATPase hydro-kali) lên các tế bào thành.
Ở ΑMAG giai đoạn cuối hoặc tiến triển hơn, việc kiểm tra tổng thể dạ dày bằng chụp X-quang cản quang hoặc chụp X-quang có thể cho thấy không có hoặc không rõ các nếp gấp ở thân dạ dày và đáy dạ dày. Ngoài ra, các mạch máu dưới niêm mạc có thể nhìn thấy qua nội soi qua lớp niêm mạc mỏng, teo, nằm bên trên. Teo và loạn sản thường không có ở hang vị trong ΑMΑG.
Ở giai đoạn cuối ΑМΑG, các tuyến chuyển sản hoàn toàn hoặc gần như hoàn toàn thay thế các tuyến oxyntic. Trong những trường hợp cực đoan, niêm mạc trở thành dạng nhung mao, rất giống với ruột non bình thường. Các tế bào biểu mô cũng có thể xuất hiện dạng hồng cầu khổng lồ ở những bệnh nhân có ΡΑ chưa được điều trị cùng với tình trạng thiếu hụt vitamin B12. Tăng sản tế bào ECL dạng nốt hoặc dạng tuyến có thể thấy rõ.
Tỷ lệ loạn sản giả môn vị so với IM trong thân và đáy dạ dày thay đổi rất nhiều ở những bệnh nhân mắc AΜΑG và cả hai dạng đều có thể chiếm ưu thế. Sự thay đổi này phải được tính đến khi lấy và giải thích mẫu sinh thiết dạ dày. Vị trí giải phẫu chính xác của sinh thiết ở đáy/thân hoặc hang vị đòi hỏi bác sĩ nội soi phải cung cấp thông tin chính xác về các vị trí sinh thiết.
Tình trạng loạn sản thường không xảy ra hoặc chỉ nhẹ ở hang vị ở những bệnh nhân mắc AМAG, nhưng những thay đổi phù hợp với bệnh lý dạ dày phản ứng thường xuất hiện vì những lý do không rõ ràng.
Viêm dạ dày teo cơ do môi trường: Các đặc điểm bệnh lý chính trong EMAG là nhiều vùng teo cơ, loạn sản và viêm phân bố cục bộ. Theo nguyên tắc, những thay đổi này tập trung nhiều nhất ở hang vị, nhưng vị trí có thể thay đổi tùy thuộc vào giai đoạn của bệnh. Những thay đổi có thể rõ ràng hơn dọc theo độ cong nhỏ hơn tại điểm giao nhau của thân và hang vị (tức là vùng chuyển tiếp) ở những bệnh nhân mắc bệnh nhẹ hoặc giai đoạn đầu. Trong bệnh nặng hoặc tiến triển, biểu mô loạn sản có thể thay thế gần như hoàn toàn niêm mạc hang vị bình thường.
Sự tiến triển từ giai đoạn sớm đến giai đoạn tiến triển của EΜAG thường được phản ánh bằng sự di chuyển gần của vùng chuyển tiếp, có thể được chứng minh bằng sinh thiết nội soi và trong các mẫu cắt bỏ. Niêm mạc oxyntic (tức là niêm mạc của thân và đáy) tiếp giáp với vùng chuyển tiếp dần dần được thay thế bằng niêm mạc dị sản ruột và giả môn vị. Ngoài ra, niêm mạc oxyntic còn nguyên vẹn có thể mỏng đi và có số lượng tế bào thành giảm. Những thay đổi này cần được xem xét khi cố gắng phân biệt bệnh lý giữa ЕΜAG và AМAG trên các mẫu sinh thiết dạ dày. Có thể nhìn thấy mô hình nhung mao màu trắng khi nội soi, đặc biệt là khi sử dụng các phương thức chụp ảnh tiên tiến như nội soi hình ảnh dải hẹp.
Xét nghiệm: Xét nghiệm huyết thanh đối với cả kháng thể kháng yếu tố nội tại và kháng thể kháng tế bào thành và nồng độ gastrin lúc đói được khuyến cáo là xét nghiệm bổ sung cho chẩn đoán mô học của ΑMΑG. Kháng thể kháng yếu tố nội tại có độ đặc hiệu cao đối với AΜAG nhưng thiếu độ nhạy . Kháng thể kháng tế bào thành có độ đặc hiệu thấp hơn nhưng có độ nhạy khoảng 80 phần trăm. Sự kết hợp của hai xét nghiệm, kết hợp với nồng độ gastrin huyết thanh lúc đói cao, có thể hỗ trợ chẩn đoán ΑΜΑG ở những bệnh nhân có các đặc điểm mô học sớm/đang tiến triển.
Nồng độ pepsinogen I trong huyết thanh thấp hoặc/và tỷ lệ pepsinogen I/II thấp là xét nghiệm không xâm lấn để phát hiện bệnh nhân mắc bệnh viêm teo dạ dày mạn tính (ΕMΑG và ΑΜΑG) giai đoạn tiến triển.
Quản lý nội soi: ở những bệnh nhân bị viêm teo dạ dày mãn tính (mãn tính) vẫn còn gây tranh cãi và chưa được khuyến nghị thống nhất.
Bệnh nhân bị viêm teo dạ dày tiến triển: Khuyến cáo về theo dõi nội soi ở bệnh nhân bị viêm teo dạ dày chuyển sản (mãn tính) dựa trên mức độ teo, mức độ chuyển sản ruột và các yếu tố nguy cơ ung thư dạ dày (ví dụ: tiền sử gia đình mắc ung thư dạ dày).
- Ở những bệnh nhân bị viêm teo dạ dày giai đoạn tiến triển (thay đổi teo nghiêm trọng hoặc loạn sản ruột ở cả hang vị và thân vị, Đánh giá liên kết phẫu thuật về viêm dạ dày/Đánh giá liên kết phẫu thuật về loạn sản ruột dạ dày III/IV) không có tiền sử gia đình mắc ung thư dạ dày, chúng tôi đề xuất theo dõi nội soi ba năm một lần.
- Bệnh nhân bị viêm teo dạ dày giai đoạn tiến triển và có tiền sử gia đình mắc ung thư dạ dày có thể được hưởng lợi từ việc theo dõi chuyên sâu hơn (ví dụ: mỗi một đến hai năm sau khi chẩn đoán).
Đối với những bệnh nhân bị teo cơ nhẹ đến trung bình giới hạn ở hang vị, không khuyến cáo theo dõi vì thiếu bằng chứng hỗ trợ cho điều này. Nồng độ pepsinogen I trong huyết thanh thấp hoặc/và tỷ lệ pepsinogen I/II thấp, đặc biệt khi liên quan đến tình trạng huyết thanh âm tính với H. pylori , có thể xác định những bệnh nhân có nguy cơ ung thư dạ dày cao hơn cần được cung cấp xét nghiệm tìm kháng thể, tuy nhiên tần suất của các xét nghiệm như vậy vẫn chưa chắc chắn.
Các khuyến nghị của chúng tôi phù hợp với hướng dẫn năm 2019 của Hiệp hội Tiêu hóa Châu Âu (ESGE) về việc quản lý các tình trạng tiền ung thư biểu mô và tổn thương ở dạ dày. Hướng dẫn năm 2015 của Hiệp hội Tiêu hóa Hoa Kỳ (ASGE) không khuyến nghị giám sát tất cả bệnh nhân bị loạn sản ruột dạ dày, nhưng nêu rằng những bệnh nhân bị loạn sản ruột dạ dày có nguy cơ mắc ung thư dạ dày cao hơn do tiền sử dân tộc hoặc gia đình có thể được hưởng lợi từ việc sàng lọc.
Bệnh nhân bị thiếu máu ác tính/viêm teo dạ dày tự miễn Ở những bệnh nhân bị thiếu máu ác tính, cần tiến hành chụp X quang dạ dày trên để xác định các tổn thương phổ biến (u nguyên bào thần kinh đệm và ung thư dạ dày) tại thời điểm chẩn đoán và để phân loại mức độ nghiêm trọng của viêm teo dạ dày tự miễn (ΑMAG).
Mặc dù hướng dẫn ASGE năm 2015 không khuyến nghị giám sát nội soi thường quy sau đánh giá nội soi ban đầu, chúng tôi đề xuất theo dõi nội soi ba đến năm năm một lần ở những bệnh nhân mắc AМAG. Tuy nhiên, hiệu quả của nội soi trong việc cải thiện kết quả cho những bệnh nhân bị thiếu máu ác tính vẫn chưa rõ ràng. Các khuyến nghị của chúng tôi phù hợp với hướng dẫn ESGE năm 2019.
Diệt trừ H. pylori: Không có phương pháp điều trị cụ thể nào cho viêm teo dạ dày (mãn tính). Nếu xác định được tác nhân gây bệnh (ví dụ, H. pylori ), cần phải loại bỏ càng sớm càng tốt. Diệt trừ H. pylori có thể dẫn đến thoái triển một phần viêm teo dạ dày. Liệu việc diệt trừ H. pylori có thể ảnh hưởng đến diễn biến tự nhiên của IM dạ dày và nguy cơ ung thư liên quan hay không vẫn chưa chắc chắn. Diệt trừ H. pylori trước khi phát triển IM dạ dày lan rộng có thể có hiệu quả trong việc giảm tỷ lệ mắc ung thư dạ dày, nhưng có thể có điểm không thể quay lại trong quá trình gây ung thư do H. pylori , trùng với sự hiện diện của viêm teo dạ dày (mãn tính)
Kiểm tra bổ sung: Ngoài việc đánh giá H. pylori , bệnh nhân bị viêm teo dạ dày nên được sàng lọc các tình trạng có thể điều trị khác, chẳng hạn như thiếu vitamin B12 và sắt.
Hệ thống Y tế MEDLATEC với các chuyên gia đầu ngành về lĩnh vực Tiêu hóa chính là một địa chỉ khám tin cậy giúp chúng ta phát hiện sớm các bệnh lý để có phương án điều trị kịp thời.
Để đặt lịch khám, quý khách hàng hãy liên hệ qua tổng đài 1900 56 56 56 để được hỗ trợ.
Tài liệu tham khảo:
Quý khách hàng vui lòng lựa chọn dịch vụ y tế theo nhu cầu!
