Bác sĩ: ThS.BSNT Trần Tiến Tùng
Chuyên khoa: Truyền nhiễm
Năm kinh nghiệm: Hơn 6 năm kinh nghiệm
Nhiễm virus viêm gan B (Hepatitis B virus: HBV) là một trong những vấn đề sức khỏe toàn cầu. Theo báo cáo của Tổ chức Y tế thế giới, năm 2015 khoảng 257 triệu người nhiễm HBV trên toàn thế giới, trong đó khoảng 884.400 số người bệnh tử vong, nguyên nhân chủ yếu là tử vong do ung thư gan (40%) và sau đó là do xơ gan (30%). HBV là một trong số những virus gây viêm gan ở người, có thể gây viêm gan cấp và mạn, lây truyền qua nhiều con đường khác nhau như đường máu, mẹ truyền sang con, tiêm chích ma túy,… Việt Nam là một trong những quốc gia có tỉ lệ nhiễm HBV cao, dao động từ 10-25%, đường lây chủ yếu là lây truyền dọc mẹ truyền sang con.
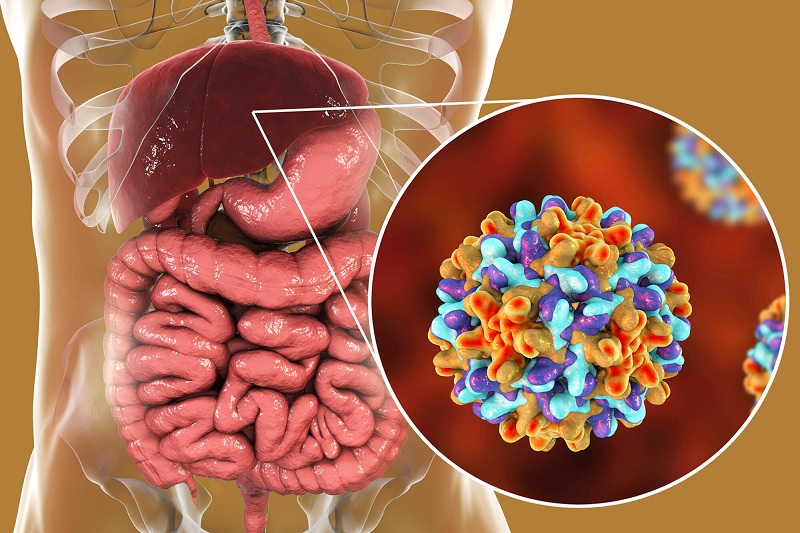
Việt Nam là một trong những quốc gia có tỉ lệ nhiễm HBV cao, tỉ lệ rơi vào khoảng 10-25%
Khi bị nhiễm HBV đa số các bệnh nhân bị viêm gan B cấp, tỉ lệ thấp hơn triến triển thành mạn tính. Mặc dù thế, viêm gan B mạn giai đoạn đầu thường ít có biểu hiện triệu chứng lâm sàng, thậm chí khi người xuất hiện biến chứng xơ gan hoặc ung thư gan mới được chẩn đoán viêm gan B mạn. Viêm gan B mạn khi có chỉ định sẽ điều trị bằng thuốc kháng virus Nucleot(s)ide analogue (NA) nhằm ức chế sự nhân lên của virus, phòng các biến chứng và hạn chế lây truyền. Việc tiêm phòng đầy đủ vắc xin viêm gan B là biện pháp quan trọng nhất để phòng lây nhiễm HBV.
Năm 1970, Dane mô tả tiểu thể virus HBV (sau này được gọi là tiểu thể Dane) hoàn chỉnh bao gồm bộ gen là một chuỗi xoắn kép ADN và ARN polymerase, bao ngoài là lớp vỏ nucleocapsid.
HBV thuộc họ Hepadnavirus, có cấu trúc hình cầu, đường kính khoảng 42 nm. Các dấu ấn sinh học của HBV gồm HBsAg, Anti HBsAg, HBcAg, Anti HBC, HBeAg, Anti HBe, HBV DNA. Ngoài ra gần đây HBcrAg còn là dấu ấn sinh học mới đang được nghiên cứu và ứng dụng trên lâm sàng đặc biệt trong quản lý và điều trị, tiên lượng bệnh. HBsAg là kháng nguyên bề mặt của HBV, nằm tại lớp vỏ virus, kháng thể tương ứng là anti HBsAg. HBcAg là kháng nguyên nhân, chỉ xuất hiện trong tế bào gan và phát hiện qua sinh thiết gan, kháng thể tương ứng là Anti HBc, trong đó HBc IgM xuất hiện sớm, còn anti HBc IgG xuất hiện muộn hơn. Kháng nguyên HBeAg là kháng nguyên xuất hiện sớm trong giai đoạn tiền vàng da, đặc biệt khi virus đang nhân lên, kháng thể tương ứng là HbeAb. HBV DNA nhằm xác định số lượng hay nồng độ của virus trong máu của người bệnh.
Virus Hepatitis B chính là nguyên nhân gây bệnh
Trong huyết thanh, HBV tồn tại dưới 02 dạng là dạng lây nhiễm (tiểu thể Dane – hạt virion) và dạng không lây nhiễm (chính là kháng nguyên bề mặt của HBV) tạo ra dư thừa trong bào tương tế bào gan.
Diễn biến tự nhiên khi nhiễm HBV mạn.
Viêm gan B mạn là hậu quả của đáp ứng miễn dịch của cơ thể với virus HBV. Diễn biến tự nhiên khi nhiễm HBV mạn tính gồm 05 giai đoạn
+ Giai đoạn dung nạp miễn dịch (nhiễm VGB mạn có HBeAg (+)): tuy HBV nhân lên mạnh trong tế bào gan, HBeAg (+), nồng độ HBV DNA cao nhưng không có triệu chứng lâm sàng, không có bằng chứng viêm gan, xét nghiệm men gan bình thường, mô bệnh học ít ghi nhân tổn thương. Nguyên nhân do sự dung nạp miễn dịch của cơ thể.
Viêm gan B sẽ có biểu hiện tùy theo giai đoạn
+ Giai đoạn thải trừ miễn dịch (VGB mạn HBeAg (+)): cơ thể có sự đáp ứng miễn dịch với HBV. Virus vẫn nhân lên nhưng bị hệ miễn dịch cơ thể tấn công. Nồng độ HBV DNA bắt đầu giảm, có bằng chứng tổn thương viêm gan trên xét nghiệm sinh hóa (men gan tăng) và mô bệnh học, cơ thể bắt đầu sinh kháng thể kháng lại HBeAg ( gọi là anti HBe), dần dần có sự chuyển đảo huyết thanh từ HBeAg dương tính sang âm tính.
+ Giai đoạn kiểm soát miễn dịch (nhiễm HBV có HBeAg (-)): nồng độ HBV DNA giảm thấp, nhiều khi không phát hiện được, sự chuyển đảo huyết thanh HBeAg rõ ràng, biểu hiện viêm gan bắt đầu thuyên giảm, men gan không còn tăng, mô bệnh học giảm mức độ hoại tử. Sự mang virus bất hoạt này có thể kéo dài nhiều năm, thậm chí suốt đời. Một số người bệnh có thể mất HBsAg, viêm gan virus B hồi phục.
+ Giai đoạn tái hoạt động (VBV mạn HBeAg (-)): Do nhiều yếu tố tác động, HBV tái hoạt trở lại mặc dù HBeAg âm tính và cơ thể đã sản sinh HBeAb. Biểu hiện viêm gan xuất hiện trở lại trên lâm sàng và xét nghiệm (men gan tăng, HCV DNA tăng trở lại).
+ Giai đoạn HBsAg âm tính (Viêm gan B thể ẩn): phân loại giai đoạn mới theo các tổ chức, hội nghị về gan mật. Một số bệnh nhân tuy xét nghiệm HBsAg âm tính, anti HBc dương tính nhưng ghi nhận HBV DNA trong huyết thanh hoặc trong tế bào gan.
Triệu chứng nhiễm HBV mạn.
Viêm gan virus B mạn tính là bệnh tiến triển thầm lặng, thời kỳ hoạt động và thời kỳ ổn định xen kẽ. Biểu hiện lâm sàng từ không có triệu chứng đến triệu chứng lâm sàng nặng, thậm chí tiên lượng tử vong cao.
Viêm gan mạn tồn tại: thường không có triệu chứng lâm sàng hoặc các triệu chứng không đặc hiệu như mệt mỏi, chán ăn, đầy bung, khó tiêu, đau tức hạ sườn phải, gan có thể to nhẹ khi thăm khám thực thể. Khi xét nghiệm men gan thường không tăng quá cao, các chức năng gan khác thường trong giới hạn bình thường. Mô bệnh học thường viêm nhẹ đại thực bào ở gan. Tiên lượng giai đoạn này thường tốt.
Viêm gan mạn hoạt động: biểu hiện lâm sàng rõ hơn, người bệnh mệt mỏi, chán ăn, ăn ngủ kém, gầy sút cân, buồn nôn, nôn, đau hạ sườn phải, vàng da, ngứa, nước tiểu, phân sẫm màu. Thăm khám thực thể thấy gan to, đau, thậm chí có thể phát hiện lách to, sao mạch, xuất huyết dưới da, cổ chướng,… Các xét nghiệm men gan thường tăng, chức năng khác của gan có thể bị giảm (albumin giảm, tỉ lệ prothrombin giảm, bilirubin tăng,…). Mô bệnh học có hoại tử tế bào gan. Bệnh tiến triển thành nhiều đợt, tiến tới xơ gan sau nhiều năm. Ở giai đoạn muộn, người bệnh có các biểu hiện xơ gan còn bù hoặc mất bù, ung thư biểu mô tế bào gan.
Virus viêm gan B tìm thấy trong máu và các dịch cơ thể. HBV lây truyền qua các con đường:

Viêm gan B có nhiều con đường lây truyền khác nhau
Bất kỳ ai chưa có miễn dịch bảo vệ đều có thể mắc viêm gan B. Khi HBsAb ≥ 10 mIU/ml thì có ý nghĩa bảo vệ. Những đối tượng nguy cơ mắc bệnh cao là:
Tiêm phòng vắc xin viêm gan B là biện pháp phòng bệnh chủ động và có hiệu quả. Tại Việt Nam việc tiêm chủng mở rộng trong đó có tiêm vắc xin viêm gan B cho trẻ em ngay sau sinh đã làm giảm tỉ lệ mắc viêm gan B xuống đáng kể. Có nhiều lại vắc xin viêm gan B như vắc xin đơn giá và đa giá. Khi tiêm đủ liều vắc xin đa số người bệnh có miễn dịch bảo vệ, Tổ chức y tế thế giới không có khuyến cáo tiêm nhắc lại.
Phòng ngừa sau khi phơi nhiễm: Gama globulin đặc hiệu với virus viêm gan B (HBIG) dùng để điều trị ngay sau phơi nhiễm với máu hoặc dịch của người mắc viêm gan B. Tiêm HBIG càng muộn càng không có hiệu quả.
Cần phải được tiêm vacxin nhanh nhất để giúp người chưa nhiễm tạo ra kháng thể
Phòng lây truyền từ mẹ sang con là biện pháp quan trọng. Trẻ sinh ra từ mẹ có HBsAg dương tính đều phải được tiêm chủng đầy đủ vắc xin viêm gan B theo chương trình tiêm chủng mở rộng. Bên cạnh đó trong 24 giờ sau sinh, trẻ cần tiêm HBIG. Khi người mẹ mang thai và có tải lượng HBV DNA > 200.000 IU/mL (> 106 copies/mL) hoặc HBsAg định lượng > 104 IU/mL, tư vấn điều trị dự phòng lây truyền HBV từ mẹ sang con bằng thuốc kháng virus TDF (tenofovir) ở tuần thứ 24 – 28 của thai kỳ, nếu phát hiện muộn hơn thì bắt đầu điều trị dự phòng ít nhất 4 tuần trước sinh và kéo dài sau sinh ít nhất 4 – 12 tuần tùy từng cá thể. Cần theo dõi sát tải lượng HBV DNA cũng như các xét nghiệm chức năng gan khác sau khi dừng thuốc. Hiện nay không có chống chỉ định nuôi con bằng sữa mẹ ở người mẹ viêm gan B mạn, tuy nhiên cần chú ý khi núm vú bị nứt, chảy máu, nhiễm trùng.
Các biện pháp phòng nguy cơ lây nhiễm khác như sàng lọc máu và các chế phẩm máu trước khi truyền, thực hiện nguyên tắc phòng chống nhiễm khuẩn bệnh viện, giáo dục và tuyên truyền an toàn tình dục.
Bệnh nhân được chẩn đoán viêm gan B mạn:
- HBsAg(+) > 6 tháng hoặc HBsAg (+) và Anti HBc IgG (+)
- AST và ALT tăng từng đợt hoặc liên tục trên 6 tháng
Có bằng chứng tổn thương mô bệnh học tiến triển, xơ gan (được xác định bằng sinh thiết gan hoặc đo độ đàn hồi gan hoặc bằng fibrotest hoặc chỉ số APRI) mà không do căn nguyên khác.
Điều trị viêm gan B mạn nhằm ức chế lâu dài sự nhân lên của HBV, từ đó cải thiện chất lượng cuộc sống, khả năng sống còn của người bệnh và góp phần phòng ngừa lây truyền HBV.
Người bệnh VGB mạn được chỉ định điều trị thuốc NAs khi nào? Lựa chọn điều trị qua 3 tiêu chí là nồng độ HBV DNA, nồng độ ALT và mức độ nghiêm trọng của bệnh gan biểu hiện trên lâm sàng, sinh thiết gan, phương pháp không xâm lấn khác. 1 số yếu tố khác cân nhắc dựa vào cá thể hóa người bệnh như tuổi, tiền sử gia đình có người bị xơ gan, ung thư gan, các biểu hiện khác ngoài gan.
Các hiệp hội gan mật tại các khu vực và thế giới có những hướng dẫn khác nhau 1 vài điểm về việc điều trị viêm gan B mạn, tuy nhiên về cơ bản việc điều trị được đánh giá trên các tiêu chí chính là HBV DNA. Nồng độ ALT và bằng chứng tổn thương gạn mạn tính. Bộ Y tế năm 2019 đã ban hành hướng dẫn chẩn đoán và điều trị viêm gan virus B trên cơ sở tham khảo những khuyến cáo trên khu vực và thế giới. Bên cạnh đó, các thuốc NAs ngày càng phát triển, không chỉ đạt được hiệu quả ức chế virus tốt còn có hàng rào kháng thuốc cao, giảm nhiều tác dụng phụ của các thuốc thế hệ trước. Hiện nay, từ năm 2015, thuốc NAs thế hệ mới TDF (tenofovir alefenamid fumarate) đã được khuyến cáo sử dụng cho bệnh nhân viên gan B mạn tại Việt Nam. Bên cạnh đó các phác đồ có Peg-IFN chỉ áp dụng đối với một số trường hợp đặc biệt. Theo Bộ Y tế năm 2019, điều trị viêm gan B mạn khi:
Đối với người bệnh có HBeAg dương tính
Đối với người bệnh có HBeAg âm tính
Khi không đủ tiêu chuẩn 2 trường hợp trên, cân nhắc điều trị khi người bệnh: Trên 30 tuổi có tăng ALT kéo dài (tăng ít nhất 3 lần trong 24 -48 tuần) và HBV DNA > 20.000 IU/ml bất kể HBeAg âm tính hay dương tính; hoặc gia đình có người bị xơ gan/HCC; hoặc lâm sàng có các biểu hiện ngoài gan như viêm cầu thận, viêm đa khớp, cryoglobulin máu,… hoặc điều trị khi người bệnh sau khi dừng thuốc NAs bị tái phát.
Các thuốc NAs có thể được dùng là: Tenofovir disoproxil fumarate (TDF) liều thường dùng với người lớn là 300 mg/ngày, chỉnh liều khi có suy giảm chức năng thận; Tenofovir alafenamide (TAF) liều thường dùng là 25 mg, không cần chỉnh liều đối với người bệnh suy giảm chức năng thận hoặc chạy thận, Entecavir (ETV) liều thường dùng là 0,5mg/ngày, chỉnh liều khi có suy giảm chức năng thận.

Người bệnh cần tuân thủ tuyệt đối phác đồ điều trị
Điều trị thuốc NAs kéo dài suốt đời đối với bệnh nhân xơ gan. Có thể cân nhắc dừng thuốc NAs ở bệnh nhân không có xơ gan khi: có chuyển đổi huyết thanh HBeAg và tải lượng HBV DNA dưới ngưỡng hoặc mất HBsAg hoặc HBcrAg âm tính. Cần theo dõi sát lâm sàng, tải lượng HBV DNA và chức năng gan sau khi ngừng điều trị.
Điều trị viêm gan B mạn ở một số cơ địa đặc biệt:
+ Đồng nhiễm HCV: chỉ định điều trị HBV mạn, HCV mạn như thông thường. Tuy nhiên khi chưa đủ tiêu chuẩn điều trị HBV mạn cần theo dõi sát lâm sàng, HBV DNA, chức năng gan. Khi tải lượng HBV DNA gấp 10 lần hoặc > 1000 IU/ml cân nhắc điều trị.
+ Phụ nữ có thai: dùng TDF khi đủ tiêu chuẩn điều trị, nếu đang điều trị viêm gan B mạn bằng các thuốc NAs khác thì thay thế bằng TDF.
+ Trẻ em: chỉ định điều trị khi trẻ ≥ 12 tháng tuổi. Dùng TDF hoặc ETV chỉnh liều theo cân nặng.
+ Bệnh nhân nhiễm HIV: nếu phác đồ ARV có TDF hoặc TAF cần tiếp tục điều trị nếu không có chỉ định đổi phác đồ ARV.
+ Ung thư biểu mô tế bào gan có HBsAg (+): điều trị các thuốc NAs lâu dài trước, trong và sau khi điều trị ung thư gan.
+ Người bệnh dùng thuốc ức chế miễn dịch, hóa trị liệu: Điều trị bằng thuốc NAs trước, trong và ít nhất 12 tháng sau khi ngưng điều trị thuốc ức chế miễn dịch, hóa trị liệu.
Cần theo dõi định kỳ chức năng gan, thận, tải lượng HBV DNA, sự chuyển đảo huyết thanh HBeAg, chuyển đảo huyết thanh HBsAg định kỳ. Bên cạnh đó cần theo dõi đánh giá thất bại điều trị, giải trình tự gen để xác định vùng đột biến kháng thuốc để cân nhắc tiếp tục phác đồ ban đầu hay thay đổi phác đồ.
Quý khách hàng vui lòng lựa chọn dịch vụ y tế theo nhu cầu!
