Bác sĩ: ThS.BS Dương Thị Thuỷ
Chuyên khoa: Nhi khoa
Năm kinh nghiệm: 15 năm
U lympho Hodgkin (HL; trước đây được gọi là bệnh Hodgkin) là bệnh ác tính huyết học trong đó các tế bào đơn nhân và đa nhân đặc trưng, lớn, loạn sản được bao quanh bởi các hỗn hợp biến đổi của các tế bào trưởng thành, không phải tân sinh, viêm và xơ.
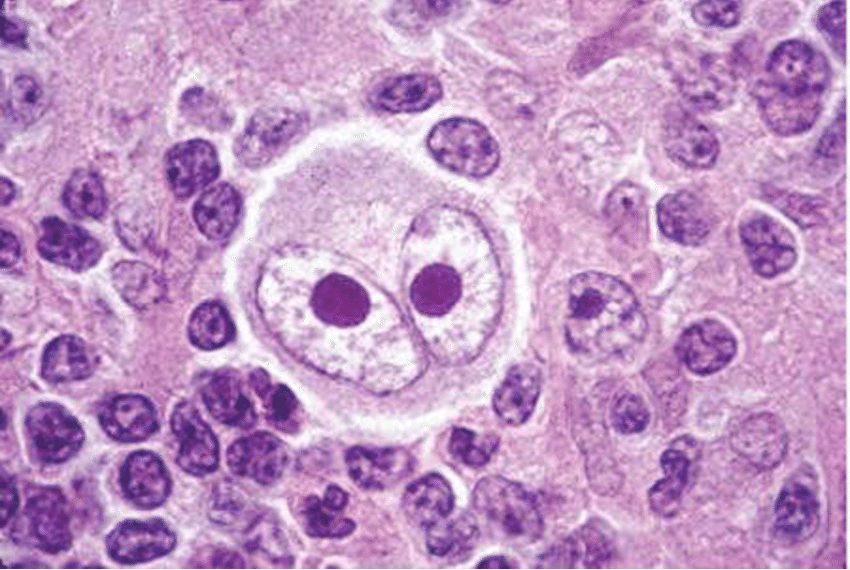
U lympho Hodgkin là bệnh ác tính huyết học
Có hai loại chính của HL: HL cổ điển (cHL) chiếm khoảng 90 phần trăm ung thư hạch Hodgkin, trong khi HL chiếm ưu thế tế bào lympho (NLPHL) chiếm phần còn lại của các trường hợp. Tuy nhiên, sự phân bố các phân nhóm mô học của cHL thay đổi tùy theo địa lý, các yếu tố kinh tế xã hội, chủng tộc / dân tộc và tuổi tác.
Tại Hoa Kỳ, Châu Âu và các khu vực kinh tế phát triển khác, HL chiếm khoảng 10% tổng số u lympho (phần còn lại là u lympho không Hodgkin), 0,6% của tất cả các bệnh ung thư và 0,2% của tất cả các trường hợp tử vong do ung thư . Tỷ lệ mắc bệnh HL ở những nơi như vậy đã ổn định ở mức 2 đến 3 trường hợp trên 100.000 người trong nhiều thập kỷ; ở Hoa Kỳ, con số này tương ứng với khoảng 8500 trường hợp mới mắc bệnh HL hàng năm, nhưng khoảng 1100 trường hợp tử vong hàng năm cho thấy tỷ lệ tử vong đang giảm dần.
Sự phân bố của các phân nhóm cHL khác nhau ở các môi trường khác và các yếu tố góp phần bao gồm các yếu tố kinh tế xã hội, độ tuổi tiếp xúc với vi rút Epstein-Barr (EBV) và tỷ lệ hiện nhiễm HIV / AIDS.
HL có phân bố theo tuổi theo hai phương thức, với đỉnh cao ở cuối tuổi vị thành niên / thanh niên và cao điểm thứ hai ở người lớn tuổi. Tuy nhiên, sự phân bố tuổi của bệnh nhân khác nhau dựa trên phân loại mô học:
- HL chiếm ưu thế tế bào lympho (NLPHL) có tỷ lệ mắc cao nhất trong thập kỷ thứ tư và thứ năm của cuộc đời, nhưng cũng gặp ở trẻ em. NLPHL phổ biến ở nam hơn nữ.
- U lympho Hodgkin cổ điển (cHL): Sự phân bố tuổi và giới tính thay đổi theo phân nhóm cHL. NSCHL có tần suất cao nhất trong độ tuổi từ 15 đến 35, trong khi MCCHL có phân bố theo hai phương thức với đỉnh ở người trẻ và đỉnh thứ hai ở người lớn tuổi. Đối với NSCHL, tỷ lệ mắc bệnh là tương đương giữa nam và nữ, nhưng nam giới chiếm ưu thế so với các phân nhóm khác của cHL
Tỷ lệ mắc HL thay đổi tùy theo chủng tộc. Ví dụ, tỷ lệ mắc bệnh ngang nhau ở người Mỹ da trắng và da đen ở Hoa Kỳ (3,1 trường hợp trên 100.000 nam giới), nhưng tỷ lệ này thấp hơn ở người Mỹ gốc Tây Ban Nha (2,6), người Châu Á / Đảo Thái Bình Dương, người Mỹ da đỏ và người bản địa Alaska.
Ngày nay, nguyên nhân gây bệnh u lympho Hodgkin vẫn chưa được làm rõ.
Nguyên nhân gây bệnh u lympho Hodgkin vẫn chưa được làm rõ
Cơ chế bệnh sinh của cHL - Các cơ chế góp phần vào quá trình sinh bệnh của cHL bao gồm:
- Các đột biến làm biến đổi tế bào lympho B khi chúng đang trong quá trình trưởng thành.
- Tín hiệu tự tiết và nội tiết không bình thường bởi các tế bào HRS (ví dụ, NF-kB, JAK-STAT) thu hút các tế bào viêm, do đó hỗ trợ sự tăng sinh và tồn tại của các tế bào HRS.
- Sự khuếch đại gen liên quan đến nhiễm sắc thể 9p24.1 dẫn đến việc bãi bỏ quy định của ít nhất bốn gen ( JAK2, JMJD2C, PDL1 và PDL2 ) quan trọng trong cơ chế bệnh sinh của HL.
- Tránh tế bào miễn dịch.
- Virus Epstein-Barr (EBV) hiện diện trong một tập hợp con các tế bào cHL và nó góp phần vào quá trình sinh bệnh bằng cách tăng cường sự phát triển và / hoặc ức chế quá trình apoptosis.
U lympho Hodgkin chiếm ưu thế tế bào lympho (NLPHL) : một phần giống với cHL các đặc điểm của tín hiệu không bình thường (ví dụ: NF-kB), kiểu hình kháng dị ứng và mất một phần kiểu hình tế bào B. Tuy nhiên, cơ chế bệnh sinh của NLPHL ít được xác định rõ ràng, đặc biệt là về cơ chế né tránh miễn dịch, bởi vì các tế bào LP không biểu hiện các phối tử PD-1.
Các tế bào chiếm ưu thế lympho bào ác tính (LP) của NLPHL có nguồn gốc từ các tế bào trung tâm B (GCB) mầm. Tế bào LP thường được tìm thấy trong các nang tế bào B mở rộng có nhiều tế bào đuôi gai và một quần thể tế bào T CD3 +, CD4 +, CD57 + đặc biệt. Tế bào LP dường như phụ thuộc vào tín hiệu của thụ thể immunoglobulin (Ig) để tăng trưởng và tồn tại.
Một số yếu tố nguy cơ:
- Tỷ lệ mắc và phân bố các phân nhóm mô học HL bị ảnh hưởng bởi địa lý, các yếu tố kinh tế xã hội, nhiễm HIV và tiền sử gia đình. Mặc dù vi-rút Epstein-Barr (EBV) có liên quan đến cơ chế bệnh sinh của HL, vi-rút này chỉ được phát hiện trong một nhóm nhỏ các trường hợp và nguy cơ tuyệt đối đối với HL sau khi nhiễm EBV là rất nhỏ.
- Việc phát hiện EBV trong tế bào Hodgkin / Reed-Sternberg (HRS) thay đổi theo phân nhóm mô học, vị trí địa lý và khả năng miễn dịch của bệnh nhân. EBV thường được kết hợp với các loại phụ MCCHL và LDCHL, phổ biến hơn ở những cơ sở hạn chế về nguồn lực và gần như luôn được phát hiện ở HL của bệnh nhân nhiễm HIV.
Chỉ một số rất nhỏ bệnh nhân bị nhiễm EBV sẽ phát triển HL. Khoảng 90 đến 95 phần trăm người lớn trên toàn thế giới có huyết thanh dương tính với EBV, nhưng tuổi nhiễm bệnh thay đổi theo điều kiện kinh tế xã hội. EBV là nguyên nhân gây ra bệnh tăng bạch cầu đơn nhân nhiễm trùng (IM), và một nghiên cứu ước tính rằng nguy cơ tuyệt đối phát triển HL sau IM là khoảng 1 trên 1000. Trong nghiên cứu bệnh chứng này, có sự gia tăng nguy cơ tương đối (RR) phát triển EBV dương tính sau IM (RR 4,0; KTC 95% 3,4-4,5), nhưng không tăng nguy cơ HL âm tính với EBV. Có thể có nguy cơ phát triển cHL dương tính với EBV cao hơn ở những bệnh nhân có một số đặc điểm di truyền nhất định.
- Các bệnh nhiễm trùng khác: Có tranh cãi về vai trò có thể có đối với herpesvirus 6 ở người (HHV6) trong cơ chế bệnh sinh của HL, nhưng hiện chưa có bằng chứng thuyết phục rằng các loại nhiễm trùng khác có vai trò nhân quả đối với HL. HHV6 được phát hiện trong tế bào HRS của khoảng một nửa số mẫu NSCHL trong một nghiên cứu, dựa trên kỹ thuật phát hiện miễn dịch và phân tử trên các tế bào bị tổn thương siêu nhỏ; HHV6 thường được tìm thấy ở những bệnh nhân trẻ hơn mắc bệnh EBV âm tính. Các nghiên cứu khác cũng đã báo cáo mối liên quan với HHV6 dựa trên huyết thanh học và các kỹ thuật khác, nhưng sự đóng góp của nó vào cơ chế bệnh sinh của HL là không rõ ràng.
- Không có bằng chứng cho thấy cytomegalovirus, virus herpesvirus 7 và 8 ở người, virus polyoma JC, adenovirus loại 5 và 12, và retrovirus 5 ở người có trong HRS. Một số bệnh truyền nhiễm ở trẻ em, bao gồm thủy đậu, sởi, quai bị, rubella và ho gà, có liên quan tiêu cực đến nguy cơ mắc bệnh HL. Một nghiên cứu bệnh chứng dựa trên dân số lớn từ Thụy Điển đã báo cáo mối liên quan giữa HL và một số bệnh nhiễm trùng nhất định (ví dụ: viêm xoang, lao, viêm não, herpes zoster), nhưng điều này có thể phản ánh tình trạng suy giảm miễn dịch cơ bản liên quan đến HL chứ không phải là nguyên nhân gây ra các bệnh nhiễm trùng này.
- Địa lý và tình trạng kinh tế xã hội: Sự phân bố của các kiểu phụ HL thay đổi theo địa lý và các yếu tố kinh tế xã hội nhất định.
Sự phân bố của các loại phụ mô học và độ tuổi dường như song song với mức độ phát triển công nghiệp ở các khu vực địa lý khác nhau.
- Các yếu tố môi trường khác: Mặc dù các yếu tố môi trường khác có liên quan đến tỷ lệ mắc bệnh HL, nhưng không có mối quan hệ nhân quả nào được chứng minh và một số yếu tố này có thể liên quan đến tình trạng kinh tế xã hội.
- Chế độ ăn, trọng lượng cơ thể: Tăng nguy cơ HL liên quan đến béo phì, dựa trên các nghiên cứu dựa trên dân số và phân tích tổng hợp. Ăn nhiều thịt hoặc đồ ngọt có liên quan đến việc tăng nguy cơ cHL. Mối liên quan tích cực giữa không hoạt động thể chất và nguy cơ mắc bệnh HL đã được báo cáo ở 87 bệnh nhân có HL so với nhóm chứng không bị ung thư.
- Aspirin: Tác dụng bảo vệ của aspirin đối với sự phát triển HL đã được báo cáo, nhưng kết quả khác nhau giữa các nghiên cứu.
- Cân nặng lúc sinh / cho con bú: Cân nặng lúc sinh cao (sau khi điều chỉnh thứ tự sinh, tuổi mẹ lúc sinh và tuổi mẹ) có liên quan đến tăng nguy cơ HL ở trẻ em (OR 1,23; KTC 95% 1,02-1,48) [ 55 ]. Tác dụng bảo vệ của việc nuôi con bằng sữa mẹ đã được chứng minh trong nhiều nghiên cứu, nhưng không biết liệu điều này có liên quan đến các kháng thể mẹ truyền hay không.
- Hút thuốc lá: Một phân tích tổng hợp phân tích 50 nghiên cứu với gần 5000 trường hợp HL báo cáo rằng tiền sử từng hút thuốc có liên quan đến tăng nguy cơ mắc bệnh HL (ước tính tác động gộp = 1,15, KTC 95% 1,02-1,30); Các mối liên hệ khá lớn đã được quan sát thấy liên quan đến cả hai kiểu phụ NSCHL và MCCHL. Một số nghiên cứu riêng lẻ sử dụng các phương pháp khác nhau đã báo cáo mối liên quan giữa hút thuốc và tỷ lệ mắc bệnh HL.
- Ức chế miễn dịch: Tỷ lệ mắc bệnh HL tăng lên ở bệnh nhân nhiễm HIV và ở các cơ sở khác có liên quan đến suy giảm miễn dịch. HL trong những quần thể này hầu như dương tính với EBV. Mặc dù có sự gia tăng tỷ lệ HL ở những người bị nhiễm AIDS, nhưng HL không được coi là một bệnh ác tính xác định AIDS. Nguy cơ tương đối của HL đã được báo cáo là tăng từ 5 đến 25 lần ở những bệnh nhân nhiễm HIV. Nguy cơ đối với HL cũng tăng lên ở những bệnh nhân sau khi ghép tạng rắn, ghép tế bào tạo máu và điều trị bằng thuốc ức chế miễn dịch (ví dụ, đối với các bệnh tự miễn).
- Rối loạn tự miễn dịch: Bệnh nhân có tiền sử rối loạn tự miễn dịch có nguy cơ phát triển HL cao hơn, nhưng không rõ liệu điều này có liên quan trực tiếp đến những tình trạng này hay nó tăng lên do các tác nhân ức chế miễn dịch được sử dụng để điều trị họ.
- Nguy cơ gia đình: Có khuynh hướng gia đình đối với HL, nhưng không rõ mức độ ảnh hưởng của tác động này là di truyền so với môi trường. Nguy cơ gia tăng ở những người thân ruột thịt của bệnh nhân HL cao hơn khoảng ba đến năm lần so với tỷ lệ dự kiến nói chung, nhưng nguy cơ có thể thay đổi theo kiểu phụ. Trong một nghiên cứu dựa trên sổ đăng ký, SIR cho cHL là 5,3 (95% CI, 3,0 đến 8,8) và SIR cho NLPHL là 19 (95% CI, 8,8 đến 36) ở thân nhân cấp độ một của bệnh nhân HL. Nguy cơ đối với HL ở anh chị em cao hơn ở cha mẹ.
- Đặc điểm di truyền: Mối liên quan nhất quán giữa di truyền với nguy cơ HL là sự biến đổi ở phức hợp tương hợp mô chính (MHC) / locus kháng nguyên bạch cầu người (HLA). Tuy nhiên, nguy cơ tăng đối với HL rất có thể là do đồng di truyền của nhiều alen nguy cơ, chứ không phải là một yếu tố quyết định di truyền duy nhất.

Yếu tố di truyền có thể là nguyên nhân gây U lympho Hodgkin
- Sự thay đổi ở các locus MHC / HLA cụ thể có liên quan đến việc tăng nguy cơ phát triển HL. Có một mối liên quan nhất quán với HLA-A1, và ở mức độ thấp hơn, HLA-B5, HLA-B8 và HLA-B18. Các nghiên cứu liên kết toàn bộ gen (GWAS) đã xác định các biến thể MHC cụ thể có liên quan độc lập với cả cHL âm tính và EBV dương tính với EBV, trong khi một số biến thể MHC nhất định được liên kết độc lập với chỉ cHL dương tính EBV và các biến thể khác chỉ liên quan đến EBV- cHL âm tính. Chưa có sự xác định nhất quán về các locus di truyền khác như là các yếu tố nguy cơ của HL.
cHL nói chung tiến triển chậm, nhưng nhịp độ của bệnh có thể thay đổi. Nổi hạch, triệu chứng toàn thân, mệt mỏi và / hoặc ngứa thường được ghi nhận là bắt đầu từ vài tuần đến vài tháng trước khi bệnh nhân được đánh giá về cHL. Các khối trung thất có thể khá lớn trước khi gây khó chịu ở ngực hoặc các triệu chứng hô hấp, phù hợp với tốc độ phát triển chậm.
Các khối trung thất có thể khá lớn trước khi gây khó chịu ở ngực hoặc các triệu chứng hô hấp, phù hợp với tốc độ phát triển chậm
Biểu hiện điển hình - Hầu hết bệnh nhân cHL có biểu hiện nổi hạch không triệu chứng hoặc một khối trên X-quang ngực. Các triệu chứng toàn thân (triệu chứng "B", tức là sốt, đổ mồ hôi ban đêm hoặc sụt cân ngoài ý muốn) có trong khoảng 40 phần trăm các trường hợp.
Trong một số ít trường hợp, biểu hiện lâm sàng của cHL tương đối không đặc hiệu hoặc không điển hình.
Hạch - Hạch có thể được phát hiện ở hơn 2/3 số bệnh nhân mắc cHL lúc chẩn đoán và các hạch bạch huyết liên quan thường không to và có độ đặc chắc, cao su. Cổ là vị trí liên quan phổ biến nhất, vì 60 đến 80 phần trăm bệnh nhân có hạch vùng cổ và / hoặc hạch thượng đòn. Các hạch nách được tìm thấy ở khoảng 30 phần trăm và các hạch ở bẹn ở 10 phần trăm bệnh nhân. Mặc dù chúng không thể phát hiện được khi khám sức khỏe, các hạch trung thất có liên quan đến 50 đến 60% và các hạch sau phúc mạc ở 30% bệnh nhân.
Đa số tiến triển từ một hạch bạch huyết đơn lẻ đến các hạch bạch huyết lân cận thông qua các kênh bạch huyết trước khi liên quan đến các vị trí và cơ quan xa hơn hoặc không liền kề. Có khả năng cHL có thể lây lan qua ống ngực, có thể theo cả hai hướng, mà không có sự mở rộng trên lâm sàng của các hạch trung thất.
Khối trung thất - Phát hiện khối trung thất trên phim chụp X quang ngực thường quy là một biểu hiện phổ biến khác của cHL; khối này có thể không có triệu chứng hoặc kết hợp với ho, khó thở hoặc đau ngực. Tràn dịch màng tim hoặc màng phổi là không phổ biến, ngoại trừ ở những bệnh nhân có hạch trung thất lớn và biểu hiện của hội chứng tĩnh mạch chủ trên là rất hiếm.
Các triệu chứng toàn thân ( B)- Các triệu chứng B đề cập cụ thể đến sốt, đổ mồ hôi ban đêm hoặc giảm cân liên quan đến ung thư hạch. Các triệu chứng B thường đi kèm với nổi hạch, nhưng bệnh nhân đôi khi chỉ có các triệu chứng B. Sự hiện diện của các triệu chứng B thay đổi theo giai đoạn bệnh; Các triệu chứng B xuất hiện ở <20 phần trăm bệnh nhân cHL giai đoạn I / II và lên đến một nửa số bệnh nhân mắc bệnh tiến triển.
Các triệu chứng toàn thân được định nghĩa chính thức như sau:
- Sốt - Nhiệt độ liên tục> 38 ° C (> 100,4 ° F)
- Đổ mồ hôi - Sự xuất hiện của đổ mồ hôi ban đêm
- Giảm cân - Giảm> 10% trọng lượng cơ thể không giải thích được trong sáu tháng qua
Các triệu chứng khác (ví dụ, mệt mỏi, ngứa, đau liên quan đến rượu) không được coi là các triệu chứng B.
Sốt kèm theo cHL thường dễ nhận thấy hơn vào buổi tối và trở nên trầm trọng hơn và liên tục theo thời gian. Sốt Pel-Ebstein đề cập đến một biểu hiện không phổ biến nhưng đặc trưng, trong đó sốt tăng theo chu kỳ và sau đó giảm trong khoảng thời gian từ một đến hai tuần
Ngứa - Ngứa xảy ra ở khoảng 10 đến 15 phần trăm bệnh nhân khi đến khám và có thể có trước chẩn đoán cHL vài tháng, thậm chí một năm hoặc lâu hơn. Ngứa thường toàn thân và đôi khi đủ nghiêm trọng để gây ra tình trạng gãi dữ dội và nổi da gà. Ngứa không được coi là một triệu chứng B.
Các biểu hiện ít phổ biến hơn - Các biểu hiện không điển hình có thể gặp ở bất kỳ bệnh nhân nào, nhưng phổ biến hơn ở những người bị nhiễm vi rút gây suy giảm miễn dịch ở người (HIV) hoặc những bệnh nhân bị ức chế miễn dịch khác
- Hiếm khi bệnh nhân cHL phàn nàn về cơn đau dữ dội sau khi uống rượu. Cơn đau thường bắt đầu trong vòng vài phút sau khi uống một lượng nhỏ rượu.
- Bệnh gan với biểu hiện như đau bụng, buồn nôn, chán ăn, các phát hiện không đặc hiệu khác.
- Nổi hạch sau phúc mạc có thể gây khó chịu hoặc đau ở mạn sườn..
- Tổn thương da - Tổn thương da được mô tả có liên quan đến cHL bao gồm bệnh đốm da, bệnh acrokeratosis (hội chứng Bazex), mày đay, hồng ban đa dạng, ban đỏ nốt sần, tổn thương hoại tử, tăng sắc tố và thâm nhiễm da
- Sự tham gia trực tiếp của hệ thần kinh trung ương (CNS) bởi cHL là rất hiếm (ví dụ: ≤0,5 phần trăm khi xuất hiện), bao gồm thoái hóa tiểu não, múa giật, suy nhược thần kinh, viêm não chi, bệnh thần kinh cảm giác bán cấp, bệnh thần kinh vận động dưới bán cấp và hội chứng cứng người đã được mô tả liên quan đến cHL.
- Hội chứng thận hư có thể xảy ra như một hội chứng paraneoplastic ở bệnh nhân cHL giai đoạn đầu. Hình thái bệnh lý thông thường là bệnh thay đổi tối thiểu, nhưng bệnh xơ cứng cầu thận phân đoạn khu trú, cũng có thể xảy ra.
NLPHL thường biểu hiện dưới dạng bệnh lý hạch ngoại vi mãn tính, không triệu chứng có thể phát hiện được bằng khám sức khỏe. Các triệu chứng liên quan đến trung thất, lách, gan và tủy xương và các triệu chứng toàn thân (B) là không phổ biến. Hầu hết bệnh nhân biểu hiện bệnh ở giai đoạn đầu (tức là giai đoạn I hoặc II).
Những người sống sót sau HL có nguy cơ phát triển các biến chứng liên quan đến điều trị có thể xuất hiện nhiều năm sau khi điều trị (ví dụ, khối u ác tính thứ hai, bệnh tim, suy giáp do bức xạ).
Biến chứng bệnh: di căn, tử vong.
- Sự phân bố của các kiểu phụ HL thay đổi theo địa lý và trình độ phát triển kinh tế. Trong các cơ sở kinh tế phát triển, NSCHL là loại phụ chiếm ưu thế, tiếp theo là MCCHL, trong khi LRCHL và LDCHL không phổ biến.
- HL thường có phân bố theo tuổi theo hai phương thức với đỉnh cao là khoảng 20 tuổi và 65 tuổi, nhưng tỷ lệ mắc và phân bố tuổi điển hình của các loại HL thay đổi theo kiểu phụ mô học và địa lý.
Tỷ lệ mắc và phân bố tuổi điển hình của các loại HL thay đổi theo kiểu phụ mô học và địa lý
- Virus Epstein-Barr (EBV) có liên quan đến sự phát triển của HL, nhưng EBV chỉ được tìm thấy trong một nhóm nhỏ các trường hợp HL; sự tham gia của EBV thay đổi theo độ tuổi, địa lý, dân tộc và loại phụ mô học. Nhiễm EBV phổ biến hơn ở những cơ sở nghèo nàn về nguồn lực và hầu như có liên quan đến HL ở những người suy giảm miễn dịch (ví dụ, HIV / AIDS).
- Các yếu tố nguy cơ khác có liên quan đến HL bao gồm tình trạng kinh tế xã hội, ức chế miễn dịch và nguy cơ gia đình / di truyền.
Hiện nay bệnh U lympho Hodgkin chưa có phòng bệnh đặc hiệu.
- Phát hiện và điều trị trường hợp nhiễm bệnh HIV, EBV.
- Quan hệ tình dục an toàn, không hút thuốc lá.
- Nuôi con bằng sữa mẹ, quản lý thai nghén tốt.
- Một lối sống lành mạnh (hạn chế dầu mỡ, thịt đỏ, đồ ngọt, không hút thuốc lá…) góp phần phòng tránh bệnh tật cũng khám sức khỏe định kỳ để phát hiện sớm bệnh.

Duy trì một lối sống lành mạnh góp phần phòng tránh bệnh tật cũng khám sức khỏe định kỳ để phát hiện sớm bệnh
Để chẩn đoán bệnh cần hỏi bệnh và thăm khám tỉ mỉ:
- Bệnh sử nên đánh giá sự hiện diện, thời gian và mức độ của bệnh lý nổi hạch; ho hoặc các triệu chứng hô hấp khác; và sốt không rõ nguyên nhân, đổ mồ hôi, sụt cân, ngứa và đau do rượu. Điều quan trọng là phải ghi lại tiền sử cá nhân về bệnh ác tính trước đây (bao gồm cả các u lympho khác); điều trị trước bằng hóa trị hoặc xạ trị; nhiễm vi rút suy giảm miễn dịch ở người (HIV) hoặc tình trạng ức chế miễn dịch khác; hoặc tiền sử gia đình về tăng sinh bạch huyết, tăng sinh tủy hoặc các khối u ác tính khác.
- Thăm khám cần đánh giá tất cả các vùng lympho có thể tiếp cận được, bao gồm kích thước, số lượng và các vùng mở rộng hạch bạch huyết, và sự hiện diện của lách to hoặc gan to. Nên khám vòng Waldeyer (amidan, đáy lưỡi, vòm họng), đặc biệt ở những bệnh nhân có hạch ở cổ.
Xét nghiệm cần làm:
- Công thức máu toàn bộ (CBC) với số lượng khác biệt và tốc độ lắng hồng cầu (ESR).
- Hóa chất trong huyết thanh, bao gồm điện giải, xét nghiệm chức năng gan và thận, và albumin.
- Xét nghiệm HIV, viêm gan B, viêm gan C, EBV.
Chẩn đoán hình ảnh:
- Đánh giá chức năng tim và phổi.
- Chụp cắt lớp phát xạ Positron / chụp cắt lớp vi tính (PET / CT).
- Trong một số trường hợp được chọn, CT chẩn đoán, chụp cộng hưởng từ (MRI), chụp X quang phổi và / hoặc các thủ thuật khác có thể được sử dụng trong HL phân giai đoạn.
Chụp CT chẩn đoán giai đoạn tiến triển bệnh
Sinh thiết mô
Được yêu cầu để chẩn đoán cHL và xác định loại mô bệnh học. Nói chung, sinh thiết ngoại vi hạch bạch huyết ngoại vi được ưu tiên hơn, nhưng sinh thiết kim nhiều lõi có thể phù hợp. Tuy nhiên, chọc hút bằng kim nhỏ (FNA) thường không cung cấp đủ mô cho tất cả các phân tích cần thiết và không cho phép phân loại mô học dứt điểm.
Bệnh lý hạch
- Đối với bệnh nhân không có bệnh lý hạch ngoại vi cần tiếp cận qua siêu âm, chụp cắt lớp vi tính (CT) hoặc chụp cắt lớp phát xạ positron (PET) có thể xác định vị trí đáng ngờ và / hoặc hướng dẫn sinh thiết mô.
Khối trung thất
- Đối với những bệnh nhân có khối trung thất, nhưng không có hạch khác có thể tiếp cận được qua CT ngực và / hoặc PET có thể xác định vị trí để sinh thiết.
Sinh thiết có thể tiếp cận qua da có hướng dẫn CT, sinh thiết nội phế quản hoặc thủ thuật phẫu thuật, chẳng hạn như phẫu thuật cắt trung thất trước (thủ thuật Chamberlain), nội soi trung thất hoặc nội soi lồng ngực / sinh thiết có video hỗ trợ (VATS).
Nói chung, chẩn đoán cHL nên được nghi ngờ ở một bệnh nhân nổi hạch hoặc một khối trên phim X quang phổi, có hoặc không có các triệu chứng B (tức là sốt, đổ mồ hôi, sụt cân) hoặc các triệu chứng khác. Tuy nhiên, biểu hiện lâm sàng của cHL có thể thay đổi và có thể xuất hiện với các triệu chứng không đặc hiệu, chẳng hạn như mệt mỏi, ngứa hoặc các phát hiện lâm sàng khác,như đã mô tả ở trên.
Chẩn đoán cHL yêu cầu những phát hiện hiển vi sau đây cộng với kiểu miễn dịch xác định của tế bào Hodgkin / Reed-Sternberg (HRS):
- Hạch bạch huyết: Tế bào HRS chẩn đoán trong tình trạng thâm nhiễm viêm đa hình của tế bào lympho nhỏ, bạch cầu ái toan, bạch cầu trung tính, mô bào, tế bào plasma và nguyên bào sợi, có hoặc không lắng đọng collagen và xơ hóa. Các tế bào HRS có thể là tế bào Reed-Sternberg (RS) nguyên mẫu hoặc các biến thể Hodgkin
- Chẩn đoán sự liên quan của cHL ở vị trí thứ phát (ví dụ: tủy xương, gan) yêu cầu sự hiện diện của các tế bào đơn nhân CD30 + trong một nền viêm thích hợp.
- Immunophenotype: HRS tế bào của CHL hiện CD30, nhưng không CD45 hoặc CD3. Hầu hết các trường hợp cHL biểu hiện CD15, nhưng sự vắng mặt của CD15 không loại trừ chẩn đoán HL. Tuy nhiên, sự vắng mặt của cả CD15 và CD30 chỉ ra các chẩn đoán khác.
Các đặc điểm sau đây là các thành phần của chẩn đoán NLPHL:
- Mô học: Sự hiện diện của các tế bào chiếm ưu thế tế bào lympho (LP) tân sinh trong nền của mô hình phát triển nốt sần hoàn toàn hoặc một phần.
- Kiểu miễn dịch: Tế bào LP thường là CD20 +, BLC6 +, CD15- và CD30-. Một bộ đánh dấu mở rộng, bao gồm kháng nguyên màng biểu mô (EMA) và các dấu hiệu tế bào B khác, chẳng hạn như CD79a và các yếu tố phiên mã BOB-1 và OCT-2, có thể hữu ích trong những trường hợp không rõ ràng.
- Mô tế bào: Tế bào nền chủ yếu bao gồm các tế bào lympho B nhỏ; Tế bào T CD3 +, CD4 +, CD57 +; và các tế bào đuôi gai dạng nang CD21 +, CD23 +.
Phân loại HL dựa trên phân loại Lugano, được bắt nguồn từ hệ thống phân giai đoạn Ann Arbor với các sửa đổi Cotswolds:

Việc điều trị bệnh nhân ung thư hạch Hodgkin (HL, trước đây gọi là bệnh Hodgkin) chủ yếu được hướng dẫn bởi giai đoạn lâm sàng của bệnh như được xác định bởi phân loại Lugano.
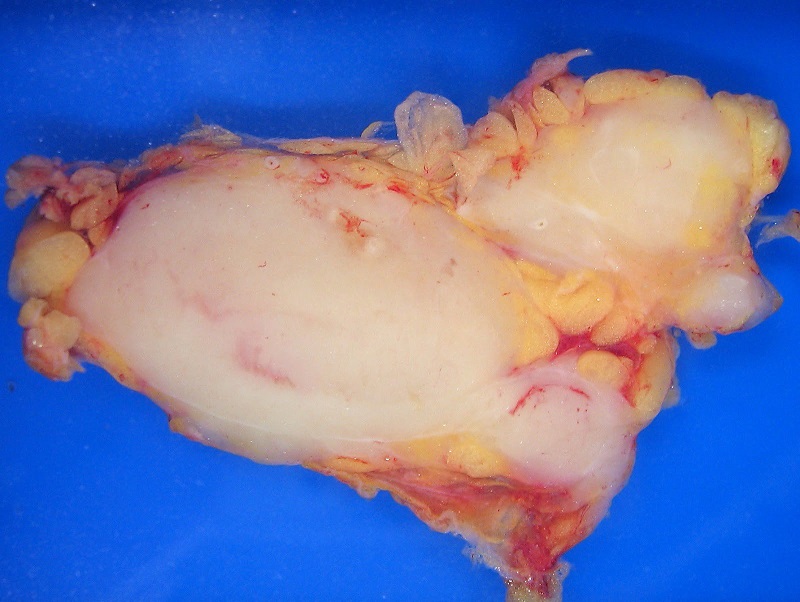
Phương pháp điều trị được căn cứ vào tình trạng và giai đoạn của bệnh
Trong khi phần lớn bệnh nhân sẽ được chữa khỏi ung thư hạch, các độc tính liên quan đến điều trị đã trở thành một nguyên nhân cạnh tranh dẫn đến tử vong muộn. Do đó, việc lựa chọn liệu pháp phải cân bằng giữa mong muốn duy trì tỷ lệ khỏi bệnh cao và nhu cầu giảm thiểu các biến chứng lâu dài.
U lympho Hodgkin cổ điển
Bệnh nhân mắc bệnh ở giai đoạn đầu (giai đoạn I đến II) thường được điều trị kết hợp giữa hóa trị và xạ trị. Lượng hóa trị và liều xạ trị khác nhau đối với những bệnh nhân có tiên lượng bệnh thuận lợi và không thuận lợi. Hóa trị một mình là một phương pháp thay thế có thể chấp nhận được cho những bệnh nhân có đặc điểm bệnh thuận lợi có nguy cơ biến chứng cao hơn do xạ trị.
- Hóa trị phối hợp là phương pháp điều trị chính cho bệnh nhân HL giai đoạn nặng (giai đoạn III đến IV). Xạ trị có thể được sử dụng cho một số bệnh nhân được chọn để củng cố.
Bệnh nhân mắc bệnh kháng thuốc nguyên phát có thể đạt được các đáp ứng và thuyên giảm lâu dài với hóa trị liệu bậc hai kết hợp các loại thuốc không được sử dụng trong điều trị ban đầu, sau đó là hóa trị liều cao và cứu tế bào tạo máu tự thân. Bệnh nhân bị tái phát lần thứ hai hoặc bệnh tiến triển, kháng thuốc cũng là những ứng cử viên cho hóa trị liều cao và cấy ghép tế bào tạo máu tự thân.
U lympho Hodgkin chiếm ưu thế tế bào dạng nốt (NLPHL)
NLPHL giai đoạn đầu với hạch nhỏ < 10 cm, không có ảnh hưởng cơ quan khác )- xạ trị tại chỗ liên quan (ISRT) hoặc giám sát tích cực (AS) ở những cá nhân được chọn thay vì hóa trị liệu hoặc liệu pháp phương thức kết hợp (CMT; tức là liệu pháp hóa trị cộng thêm xạ trị).
NLPHL giai đoạn đầu với hạch lớn, ảnh hưởng chức năng cơ quan- hóa trị đơn thuần hoặc ISRT đơn thuần (đối với những bệnh nhân có phân bố bệnh phù hợp) hơn là CMT.
NLPHL giai đoạn sau: điều trị nên được hướng dẫn theo mức độ nghiêm trọng của các triệu chứng:
- Đối với những bệnh nhân có triệu chứng: liệu pháp hóa trị thay vì ISRT hoặc CMT.
- Không có triệu chứng hoặc ít có triệu chứng: liệu pháp hóa trị, rituximab đơn chất hoặc AS là những lựa chọn có thể chấp nhận được; lựa chọn phương pháp tiếp cận nên được cá nhân hóa để phản ánh sở thích và mối quan tâm của bệnh nhân.
Quý khách hàng vui lòng lựa chọn dịch vụ y tế theo nhu cầu!
