Tin tức
COVID-19: Vai trò của các dấu ấn Phân tử, Huyết học và Hóa sinh trong chẩn đoán, theo dõi đáp ứng điều trị và tiên lượng
- 22/02/2022 | Hệ thống Y tế MEDLATEC GROUP vinh dự nhận bằng khen của Thủ tướng Chính phủ tại Hội nghị Gặp...
- 25/02/2022 | F0 bị nhẹ bất ngờ phát hiện nhiều tổn thương phổi hậu COVID-19
- 19/02/2022 | Tiếp cận chẩn đoán - chăm sóc bệnh nhân hô hấp Hội chứng hậu COVID-19
- 26/02/2022 | Những đêm thức trắng của “Người MEDLATEC” tham gia chống dịch COVID-19
- 24/02/2022 | Hướng dẫn cách chăm sóc trẻ mắc COVID-19 tại nhà đúng và an toàn
PGS TS Nguyễn Nghiêm Luật
Bệnh viện Đa khoa MEDLATEC
Tóm tắt
1) Các dấu ấn sinh học để chẩn đoán COVID-19: Phản ứng chuỗi polymerase phiên mã ngược thời gian thực (rRT-PCR) là xét nghiệm tiêu chuẩn hiện nay để chẩn đoán, trong khi xét nghiệm kháng nguyên nhanh là xét nghiệm miễn dịch để phát hiện sự hiện diện của một kháng nguyên đặc hiệu của virus và các xét nghiệm kháng thể (huyết thanh học) là các xét nghiệm được sử dụng để phát hiện sự nhiễm SARS-CoV-2 trước đó.
2) Các dấu ấn sinh học để theo dõi đáp ứng điều trị ở bệnh nhân COVID-19: Độ chính xác của mức độ CRP và IL-6 trong dự đoán đáp ứng điều trị đã được đánh giá. Những phát hiện hứa hẹn về PT và D-dimer cũng đã được báo cáo. Tuy nhiên, hiệu quả của các dấu ấn sinh học này trong việc dự đoán đáp ứng điều trị còn ít, cần phải có thêm các nghiên cứu để xác nhận.
3) Các dấu ấn sinh học để dự đoán bệnh nặng ở bệnh nhân COVID-19: Sự thiếu máu, sự tăng của tỷ lệ bạch cầu trung tính/ tế bào lympho, tỷ lệ tiểu cầu/ tế bào lympho và mức độ D-dimer khi nhập viện có thể là những yếu tố dự báo bệnh COVID-19 nặng cần nhập viện ICU.
4) Các dấu ấn sinh học để dự đoán tử vong ở bệnh nhân COVID-19: Ở bệnh nhân tử vong, số lượng bạch cầu, số lượng bạch cầu trung tính, CRP, hsCRP, procalcitonin, ferritin, D-dimer, IL-6, PT, LDH, CK, AST, ALT, bilirubin toàn phần và creatinine cao, trong khi số lượng tế bào lympho, số lượng tiểu cầu và albumin thấp hơn một cách rõ rệt.
5) So với bệnh nhi COVID-19 ngoại trú, bệnh nhi nội trú có số lượng bạch cầu, tế bào lympho và tiểu cầu, CRP, procalcitonin, D-dimer và tỷ lệ lymphocyte trên monocyte cao hơn một cách có ý nghĩa. Trẻ bị bệnh hô hấp nặng và hội chứng viêm đa hệ thống ở trẻ em (MIS-C) có mức độ CRP, procalcitonin hoặc troponin cao hơn, trong khi số lượng tiểu cầu hoặc mức độ Natri huyết thanh thấp hơn một cách có ý nghĩa so với những trẻ bị bệnh nhẹ.
*
COVID-19: The role of Molecular, Hematological and Biochemical Markers in the diagnosis, monitoring treatment response and prognosis
Luat Nghiem Nguyen
MEDLATEC General Hospital
Abstract
1) Biomarkers for diagnosis of COVID-19: Real-time reverse transcription polymerase chain reaction (rRT-PCR) is the current standard test for diagnosis, while rapid antigen tests are immunoassays that detect the presence of a specific viral antigen and antibody (or serology) tests are used to detect previous infection with SARS-CoV-2.
2) Biomarkers for treatment response in COVID-19 patients: The accuracy of the CRP and IL-6 levels in predicting treatment responses has been evaluated. Promising findings on PT and D-dimer have also been reported. However, the efficacy of these biomarkers in predicting the treatment response are sparse, necessitating confirmatory studies.
3) Biomarkers for prediction of severe disease in patients with COVID-19: Anemia, increased neutrophil-to-lymphocyte ratio, platelet-to-lymphocyte ratio, and D-dimer level at time of admission could be available predictors for severe COVID-19 infection requiring ICU admission.
4) Biomarkers for prediction of mortality in patients with COVID-19: White blood cell count, neutrophil count, CRP, hsCRP, procalcitonin, ferritin, D-dimer, IL-6, PT, LDH, CK, AST, ALT, total bilirubin and creatinine were significantly higher, while lymphocyte count, platelet count and albumin were significantly lower in non-survivors.
5) Compared with COVID-19 outpatients, inpatients had significantly higher white blood cell, lymphocyte, and platelet counts, CRP, procalcitonin, D-dimer, and lymphocyte to monocyte ratio values. Children with severe respiratory disease and multisystem inflammatory syndrome in children (MIS-C) have significantly higher CRP, procalcitonin, or troponin level, while a lower platelet count, or serum sodium level compared to those with non-severe disease.
*
Đại dịch COVID-19 do SARS-CoV-2 gây ra lần đầu tiên xuất hiện tại Vũ Hán, Trung Quốc vào tháng 12 năm 2019, không chỉ gây ra tỷ lệ mắc bệnh toàn cầu đáng kể (tính đến 28/2/2022 là >435 triệu trường hợp) và tử vong (>5,9 triệu trường hợp tử vong), mà còn gây xáo trộn cho xã hội và nền kinh tế. Tỷ lệ thực sự của COVID-19 có thể đã bị đánh giá thấp, do các báo cáo sai các ca không triệu chứng, có triệu chứng nhẹ hoặc các ca xét nghiệm không đầy đủ. Các chiến lược sàng lọc và chẩn đoán đối với COVID-19 đã thay đổi trên toàn thế giới tùy theo các chính sách của các chính phủ, công nghệ, sự tài trợ và khả năng quản lý dữ liệu. Ngay cả ở các quốc gia công nghiệp phát triển, sự không chắc chắn trong chiến lược, các rào cản quy định và các vấn đề cung cấp đã làm gián đoạn khả năng kiểm soát, có thể góp phần làm trầm trọng thêm sự lây lan của SARS-CoV2. Việc tiêu chuẩn hóa và cải tiến chẩn đoán COVID-19, với khả năng phát hiện và điều trị các ca bệnh hiệu quả hơn, có thể có lợi cho cả các quốc gia công nghiệp hóa và các quốc gia có thu nhập thấp.
Trong bài viết này, chúng tôi đánh giá tổng quan về vai trò của các dấu ấn Phân tử, Huyết học và Hóa sinh trong chẩn đoán, theo dõi đáp ứng điều trị và tiên lượng bệnh COVID-19.
1. Các dấu ấn sinh học sử dụng trong chẩn đoán nhiễm SARS-CoV-2
Các dấu ấn sinh học có thể sử dụng trong chẩn đoán COVID-19 bao gồm SARS-CoV-2 RNA, kháng nguyên và các kháng thể IgM và IgG trong bệnh COVID-19.
Sự thay đổi mức độ RNA của SARS-CoV-2, kháng nguyên (antigen), các kháng thể của người trong quá trình nhiễm SARS-CoV-2 và quá trình hồi phục nói chung gồm 3 giai đoạn:
1) Giai đoạn ủ bệnh (không triệu trứng): thường từ 0-5 ngày sau khi nhiễm SARS-CoV-2.
2) Giai đoạn khởi phát (xuất hiện triệu chứng): từ ngày thứ 5 sau khi nhiễm SARS-CoV-2.
3) Giai đoạn hồi phục (triệu chứng giảm dần): từ ngày thứ 14 sau khi nhiễm SARS-CoV-2 và khoảng ngày thứ 10 kể từ khi xuất hiện triệu chứng.
RNA và kháng nguyên của SARS-CoV-2 xuất hiện ngay từ ngày đầu bị nhiễm virus, đạt mức cao nhất vào khoảng ngày thứ 14 rồi giảm dần và có thể biến mất vào ngày thứ 21.
Kháng thể chống SARS-CoV-2 IgM thường xuất hiện vào ngày thứ 7 sau nhiễm virus, đạt mức cao nhất vào khoảng ngày thứ 14 đến 21 rồi giảm dần và có thể biến mất vào ngày thứ 28.
Kháng thể chống SARS-CoV-2 IgG thường xuất hiện muộn hơn, thường là vào ngày thứ 14 sau nhiễm virus, đạt mức cao nhất trong vòng vài tháng tiếp theo và có thể tồn tại một thời gian dài sau đó (Hình 1).
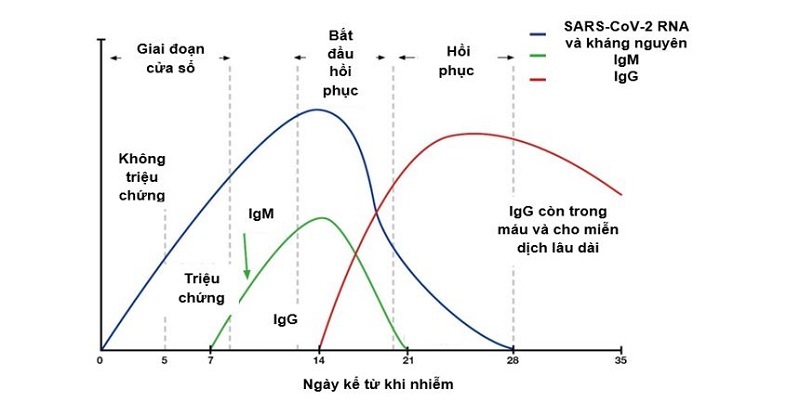
Hình 1. Sự thay đổi mức độ của SARS-CoV-2 RNA và kháng nguyên, IgM và IgG sau khi nhiễm virus (Nguồn: Diazyme Laboratories, Inc. Retrieved from http:/www.diazyme.com/covid-19-antibody-tests). Trục tung: mức độ của các thông số; trục hoành: thời gian kể từ khi bị nhiễm SARS-CoV-2 (ngày); màu xanh da trời: mức độ RNA và kháng nguyên của SARS-CoV-2; màu xanh lá cây: kháng thể IgM; màu đỏ: kháng thể IgG của người.
Sự hiểu biết về sự thay đổi mức độ RNA và kháng nguyên trong dịch hầu, họng và các kháng thể IgM và IgG trong máu ở người nhiễm SARS-CoV-2 có thể giúp thầy thuốc chỉ định các xét nghiệm và đánh giá một cách chính xác các giai đoạn của bệnh.
1.1. Xét nghiệm phân tử SARS-CoV-2
Xét nghiệm phân tử (molecular tests) là một phương pháp trực tiếp, thường sử dụng phản ứng chuỗi polymerase sao chép ngược thời gian thực rRT-PCR (real-time reverse transcription polymerase chain reaction), giúp phát hiện virus ở người bị nhiễm được dựa trên việc phát hiện RNA của SARS-CoV-2 lấy từ dịch tiết tỵ hầu. Mặc dù RT-PCR là tiêu chuẩn vàng để chẩn đoán COVID-19, nó vẫn có khả năng cho kết quả âm tính giả, điều này có thể liên quan đến tải lượng virus, thời gian lấy mẫu hoặc lấy mẫu sai. Xét nghiệm RT-PCR thường cho kết quả dương tính nếu bệnh phẩm được lấy từ 2-8 ngày sau khi bắt đầu nhiễm virus. Một phân tích tổng hợp, đánh giá độ chính xác của các xét nghiệm COVID-19 và bao gồm 34 nghiên cứu với 12.057 trường hợp được xác nhận COVID-19 đã báo cáo tỷ lệ RT-PCR âm tính giả là từ 2% đến 29%. Độ nhạy được báo cáo là 71-98%, dựa trên những cá nhân có RT-PCR âm tính ban đầu được phát hiện là có kết quả dương tính. Độ chính xác chẩn đoán COVID-19 có thể được cải thiện bằng cách kết hợp các kết quả của RT-PCR, chẩn đoán hình ảnh và huyết thanh học.
Một số phương pháp khác, như PCR kỹ thuật số giọt (droplet digital PCR: ddPCR) và khuếch đại đẳng nhiệt qua trung gian phiên mã ngược (reverse transcription-loop-mediated isothermal amplification: RT-LAMP) để phát hiện SARS-CoV-2 RNA cũng đang được sử dụng để bổ sung cho RT-PCR. Nói chung, ddPCR hoạt động tốt hơn RT-PCR tiêu chuẩn để chẩn đoán SARS-CoV-2, có thể làm giảm kết quả âm tính giả. Một nghiên cứu gần đây cho thấy sự kết hợp RT-PCR với ddPCR cho phép cải thiện độ nhạy từ 40% (95% CI: 27-55%) lên 94% (95% CI: 83-99%) mà không làm thay đổi độ đặc hiệu, là 100% (CI 95%: 48-100) (Ulinici M, 2021 [11]).
1.2. Xét nghiệm kháng nguyên SARS-CoV-2
Xét nghiệm kháng nguyên nhanh (rapid antigen tests) là một phương pháp trực tiếp, có khả năng phát hiện sự hiện diện của các protein của virus SARS-CoV-2 trong mẫu gạc và nước bọt ở tỵ hầu một cách nhanh chóng. Hầu hết xét nghiệm kháng nguyên SARS-CoV-2 là xét nghiệm miễn dịch sắc ký dòng bên (tại điểm chăm sóc, nhanh) hoặc xét nghiệm miễn dịch phát quang hóa học (dựa trên phòng thí nghiệm). Mặc dù các xét nghiệm kháng nguyên ngày càng được sử dụng nhiều hơn, nhưng độ chính xác chẩn đoán của các xét nghiệm này thấp hơn so với RT-PCR. Có một số lo ngại về tính đặc hiệu của chúng, vì chúng có thể phản ứng chéo với các coronavirus khác, nhưng vấn đề chính là độ nhạy của chúng. Xét nghiệm kháng nguyên SARS-CoV-2 có độ nhạy từ 34% đến 88%. Độ chính xác chẩn đoán của chúng cao nhất ở những bệnh nhân có triệu chứng, khi tải lượng virus trong tỵ hầu cao hơn, cho phép chẩn đoán sớm. Thời gian tối ưu của xét nghiệm có thể thay đổi (trong vòng 5, 7 và 12 ngày kể từ ngày khởi phát triệu chứng). Ưu điểm chính của xét nghiệm kháng nguyên là cho kết quả nhanh, dễ giải thích, không đòi hỏi kỹ năng cao và cơ sở hạ tầng hiện đại. Vì vậy, xét nghiệm kháng nguyên là hữu ích hơn trong việc kiểm soát sự lây lan của lây nhiễm so với xét nghiệm phân tử (Ulinici M, 2021 [11]).
WHO đã đặt ra yêu cầu về độ nhạy tối thiểu “có thể chấp nhận được” cho xét nghiệm kháng nguyên là ≥80%, độ đặc hiệu lý tưởng và chấp nhận được tương ứng là 97% và 99%.
1.3. Xét nghiệm kháng thể IgM và IgG
Xét nghiệm huyết thanh học là một phương pháp gián tiếp, có thể thay thế để chẩn đoán COVID-19, thường được sử dụng để phát hiện người đã bị nhiễm SARS-CoV-2 trước đó. Một số kỹ thuật được sử dụng để xác định các kháng thể IgG và IgM có thể gồm ELISA, xét nghiệm miễn dịch dòng chảy bên (LFIA) và xét nghiệm miễn dịch hóa phát quang (CLIA).
Độ nhạy của IgM và IgG trong những tuần đầu của nhiễm COVID-19 tương ứng là 33% và 23% ở tuần 1 và 73% và 68% ở tuần 2. Sau 3 đến 4 tuần, các xét nghiệm kháng thể IgG hoặc tổng số IgM và IgG cho độ nhạy và độ đặc hiệu cao nhất. Độ nhạy xét nghiệm kháng thể từ tuần thứ 3 sau khởi phát triệu chứng là từ 69,9% đến 98,9%, cao hơn so với ở tuần đầu tiên (13,4% đến 50,3%), trong khi độ đặc hiệu là khoảng từ 96,6% đến 99,7%. Kết quả xét nghiệm huyết thanh có thể dương tính giả khi có sự hiện diện của các nhiễm virus khác (như cytomegalovirus) hoặc các bệnh tự miễn (như xơ cứng bì hoặc lupus ban đỏ hệ thống) (Bohn MK, 2020 [3], Ulinici M, 2021 [11]).
Ý nghĩa lâm sàng của các xét nghiệm RT-qPCR, IgM và IgG trong chẩn đoán COVID-19 được thể hiện ở Bảng 1.
Bảng 1. Ý nghĩa lâm sàng của các xét nghiệm RT-qPCR, IgM và IgG trong chẩn đoán COVID-19 (Diazyme Laboratories, Inc. http:/www.diazyme.com/covid-19-antibody-tests).
|
Kết quả xét nghiệm |
Ý nghĩa lâm sàng |
||
|
RT-qPCR |
IgM |
IgG |
|
|
+ |
- |
- |
Bệnh nhân có thể ở giai đoạn cửa sổ của nhiễm |
|
+ |
+ |
- |
Bệnh nhân có thể ở giai đoạn sớm của nhiễm |
|
+ |
+ |
+ |
Bệnh nhân ở giai đoạn cấp của nhiễm |
|
+ |
- |
+ |
Bệnh nhân có thể ở giai đoạn muộn của nhiễm |
|
- |
+ |
- |
Bệnh nhân có thể ở giai đoạn sớm. RT-qPCR có thể là (-) tính giả |
|
- |
- |
+ |
Bệnh nhân có thể đã qua nhiễm, đã hồi phục |
|
- |
+ |
+ |
Bệnh nhân có thể ở giai đoạn hồi phục. RT-qPCR có thể là (-) tính giả |
Ghi chú: Sự thay đổi của kháng nguyên SARS-CoV-2 tương tự như RT-qPCR, nhưng độ nhạy kém hơn.
2. Vai trò của các dấu ấn sinh học trong đánh giá độ nặng của bệnh COVID-19
Mặc dù bệnh COVID-19 gây ra bởi virus gây hội chứng hô hấp cấp (SARS-CoV-2) đã được biết đến rộng rãi trên toàn thế giới, nhưng rất khó dự đoán bệnh sẽ biểu hiện như thế nào ở một bệnh nhân. Các biểu hiện của COVID-19 có triệu chứng rất khác nhau, từ sốt nhẹ (>37,5°C) và ho, có thể dẫn đến hội chứng suy hô hấp cấp tính (acute respiratory distress syndrome: ARDS) hoặc tử vong. Sự thay đổi này đã dẫn đến việc cần tìm kiếm các dấu ấn sinh học về mức độ nặng của bệnh để quản lý bệnh nhân một cách thích hợp và ngăn ngừa các biến chứng nặng. Bệnh COVID-19 nặng có sinh lý bệnh viêm phổ biến liên quan đến hội chứng bão cytokine (cytokine storm syndrome: CSS), gây nên bởi sự kích hoạt viêm mạnh để phản ứng với sự nhiễm virus. Ngoài ra, các tổn thương cơ quan và suy đa tạng (multi-organ failure: MOF) do viêm mạch máu thường được thấy ở bệnh nhân COVID-19. Theo đó, hầu hết các dấu ấn sinh học được khảo sát ở bệnh nhân COVID-19, như protein phản ứng C (CRP), interleukin-6 (IL-6), procalcitonin (PCT), số lượng bạch cầu (WBC), số lượng bạch cầu đa nhân trung tính (NC), số lượng tế bào lympho (LC), tỷ lệ bạch cầu đa nhân trung tính/tỷ lệ tế bào lympho (NLR), D-dimer, thời gian prothrombin (PT) và thời gian thromboplastin một phần được kích hoạt (aPTT) đều thuộc về sự viêm do miễn dịch (immune-inflammatory) và các con đường của sự đông máu (coagulation pathways). Các dấu hiệu sinh học không đặc hiệu khác của tổn thương tế bào và viêm có thể bao gồm lactate dehydrogenase (LDH) và các transaminase. Hơn nữa, COVID-19 nặng cũng thường liên quan đến các tổn thương tim, gan và thận (Bivona G, 2021 [2]). Do đó, các dấu ấn sinh học đặc hiệu cơ quan cũng đã được đánh giá ở những bệnh nhân này (Hình 2).
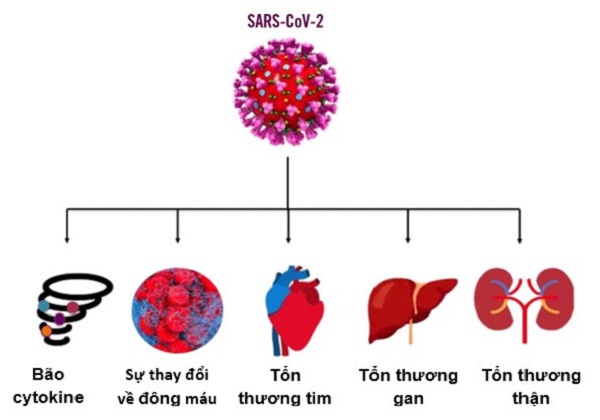
Hình 2. Những thay đổi do nhiễm SARS-CoV-2 (Bivona G, 2021 [2]).
Ngoài ra, các phân tử mới như các dấu ấn sinh học của sự nhiễm khuẩn huyết (sepsis biomarkers) và các microRNA (miRNAs), cũng được đánh giá là dấu ấn sinh học COVID-19 tiềm năng của bệnh COVID-19 (Bivona G, 2021 [2]).
2.1. Các dấu ấn sinh học sử dụng để đánh giá mức độ nặng của bệnh COVID-19
Các dấu ấn sinh học có thể được sử dụng để đánh giá mức độ nặng của bệnh, theo dõi đáp ứng điều trị và tiên lượng tử vong ở bệnh nhân COVID-19 có thể gồm:
1) Các dấu ấn về Huyết học: Sự tăng bạch cầu/ giảm bạch cầu (leucocytosis/leucopenia), sự giảm tế bào lympho (lymphopenia), sự giảm bạch cầu trung tính (neutrophilia), sự cạn kiệt (depletion) các tế bào CD4+ và CD8+, sự tăng tỷ lệ bạch cầu trung tính trên tế bào lympho (neutrophil-to-lymphocyte ratio: NLR), sự giảm tiểu cầu/ sự tăng tiểu cầu (thrombocytopenia/thrombocytosis)
2) Các dấu ấn về viêm: Các cytokine, các chemokine, các yếu tố tăng trưởng (growth factors), protein phản ứng C (CRP), procalcitonin, lactate dehydrogenase (LDH)
3) Các dấu ấn về đông máu: Mức độ D-dimer, Fibrinogen, sản phẩm thoái hóa Fibrin (FDP), thời gian prothrombin (PT), thời gian thromboplastin một phần được kích hoạt (aPTT)
4) Các dấu ấn về tổn thương mô:
• Các dấu ấn về tổn thương tim mạch: Troponin tim (cTnT), peptit natri lợi niệu não (BNP)/ NT-proBNP
• Các dấu ấn về tổn thương gan: Aspartate aminotransferase (AST), Alanine aminotransferase (ALT), Bilirubin, Albumin
• Các dấu ấn về tổn thương cơ: Creatine-kinase (CK), Myoglobin
• Các dấu ấn về tổn thương thận: Creatinine huyết thanh,
5) Các dấu ấn về điên giải: Hạ Natri máu (Hyponatremia), Hạ kali máu (Hypokalemia), Hạ calci máu (Hypocalcemia) (Samprathi M và Jayashree M, 2020 [9]).
Hiệp hội Hóa Lâm sàng và Xét nghiệm Y học Quốc tế (International Federation of Clinical Chemistry and Laboratory Medicine: IFCC) cũng còn chia các dấu ấn sinh học trong quả lý bệnh COVID-19 thành các dấu ấn Huyết học và các dấu ấn Hóa sinh.
Các dấu ấn Huyết học được IFCC khuyến nghị sử dụng ở bệnh nhân nhiễm COVID-19 được thể hiện ở Bảng 2.
Bảng 2: Các dấu ấn Huyết học được IFCC khuyến nghị sử dụng ở bệnh nhân nhiễm COVID-19 (Thompson S, 2020 [10]).
|
Xét nghiệm |
Các phát hiện |
Ý nghĩa lâm sàng |
|
Công thức máu toàn phần (CBC) |
↑ Bạch cầu trung tính ↓ Các tế bào lympho ↓ Bạch cầu ái toan |
- Tỷ lệ bạch cầu trung tính trên các tế bào lympho tăng cao có liên quan đến kết quả lâm sàng kém. - Sự giảm các tế bào lympho là một dấu ấn nhận biết trong nhiễm trùng có triệu chứng. |
|
D-dimer |
Tăng |
Để xác định những người có nguy cơ dẫn đến kết quả bất lợi. |
|
Tiểu cầu |
Giảm |
Liên quan đến kết quả lâm sàng kém. |
|
PT/aPTT |
Tăng |
Để xác định và theo dõi rối loạn đông máu |
|
Fibrinogen |
Tăng/ Giảm |
- Tăng rối loạn đông máu do COVID-19. - Giảm đông máu nội mạch lan tỏa (DIC). |
Ghi chú: PT (prothrombin time): thời gian prothrombin; aPTT (activated partial thromboplastin time): thời gian thromboplastin được hoạt hóa một phần; DIC (disseminated intravascular coagulation): đông máu nội mạch lan tỏa.
Các dấu ấn Hóa sinh được IFCC khuyến nghị sử dụng ở bệnh nhân nhiễm COVID-19 được thể hiện ở Bảng 3.
Bảng 3: Các dấu ấn Hóa sinh được IFCC khuyến nghị ở bệnh nhân nhiễm COVID-19 (Thompson S, 2020 [10]).
|
Xét nghiệm |
Các phát hiện |
Ý nghĩa lâm sàng |
|
Khí máu động mạch |
Thay đổi |
Để xác định và theo dõi tình trạng giảm oxy máu và nhiễm toan chuyển hóa liên quan đến nhiễm trùng nặng. |
|
CRP |
Tăng |
Có liên quan đến kết quả lâm sàng xấu hơn. |
|
Ferritin |
Tăng |
Ferritin tăng Có liên quan đến kết quả lâm sàng xấu hơn. |
|
Tốc độ máu lắng (ESR) |
Tăng |
Thay thế cho CRP/ ferritin trong các cài đặt giới hạn tài nguyên. |
|
Procalcitonin |
Tăng |
Liên quan đến nhiễm khuẩn thứ phát |
|
Troponin tim |
Tăng |
Liên quan đến bệnh tim do COVID-19 và tiên lượng xấu. |
|
ALT, bilirubin |
Tăng |
Cần được theo dõi ở những bệnh nhân được điều trị bằng các thuốc có ảnh hưởng đến chức năng gan (ví dụ: lopinavir/ ritonavir) |
|
Albumin |
Giảm |
Phản ánh viêm gan cấp hoặc rối loạn chức năng tổng hợp của gan. |
|
Creatinin, Urea (BUN) |
Tăng |
Liên quan đến tiên lượng xấu. |
|
IL-6 IL-10 |
Tăng |
Chỉ sử dụng trong nghiên cứu. Liên quan đến kết quả lâm sàng kém. |
Ghi chú: CRP (C-reactive protein): Protein phản ứng C; ESR (erythrocyte sedimentation rate): tốc độ máu lắng; ALT: alanin aminotransferase; BUN (blood urea nitrogen): nitơ urê máu; LDH: lactat dehydrogenase.
2.2. Những thay đổi tạm thời của các dấu ấn sinh học trong bệnh COVID-19
Những thay đổi tạm thời của các dấu ấn sinh học là các thay đổi của các dấu ấn này trong quá trình diễn biến thông thường của bệnh COVID-19 sau đó lại trở về các mức độ bình thường sau khi khỏi bệnh (Bảng 4).
Bảng 4. Những thay đổi tạm thời của các dấu ấn sinh học trong bệnh COVID-19 (Samprathi M and Jayashree M, 2020 [9]).
|
Khoảng thời gian nhiễm SARS-CoV-2 |
Những thay đổi tạm thời của các dấu ấn sinh học |
|
<7 ngày |
• Số lượng bạch cầu và số lượng tế bào lympho bình thường hoặc hơi thấp • ↑ LDH, ↑ AST, ↑ ALT, ↑ CK, ↑ CK-MB - có thể là dấu hiệu ban đầu của bệnh nặng và tử vong |
|
7-14 ngày |
• Số lượng bạch cầu và số lượng các tế bào lympho giảm dần để đạt mức độ bình thường sau 8-9 ngày • Có thể xảy ra sự giảm tiểu cầu • ↑ IL-6, IL-10, IL-1RA, MCP-1 |
|
>14 ngày |
• Sự tăng số lượng bạch cầu, tế bào lympho và tiểu cầu giúp dự đoán khả năng hồi phục, trong khi sự giảm số lượng dự đoán sự tử vong |
Ghi chú: ALT: alanin transaminase; AST: aspartate transaminase; CK: creatine kinase; IL-6: interleukin-6; LDH: lactate dehydrogenase; MCP (monocyte chemoattractant protein 1): protein 1 có ái lực hóa học với bạch cầu đơn nhân.
2.3. Vai trò của các dấu ấn sinh học sử dụng để đánh giá mức độ nặng của bệnh
Hashem MKvà cộng sự, 2021 [4], trong một nghiên cứu trên 351 bệnh nhân (+) tính với COVID-19 nhập viện, được chia loại thành bệnh nhân không nặng và nặng theo các tiêu chuẩn của đơn vị chăm sóc tích cực (Intensive Care Unit: ICU), có 145 (41,3%) bệnh nhân cần đưa vào ICU. Sự thiếu máu (anemia), sự tăng bạch cầu đa nhân trung tính (leukocytosis), sự giảm tế bào lympho (lymphopenia), tỷ lệ tỷ lệ bạch cầu trung tính trên tế bào lympho (neutrophil-to-lymphocyte ratio: NLR) và tỷ lệ tiểu cầu trên tế bào lympho (platelet-to-lymphocyte ratio: PLR), cùng với các enzym gan, INR, ferritin, CRP và D-dimer cao hơn đáng kể ở những bệnh nhân cần đưa vào ICU (p<0,001). Tuy nhiên, khi áp dụng cách tính hồi quy logistic đa biến (multivariate logistic regression) thì chỉ có sự thiếu máu, NLR cao, PLR cao và mức D-dimer cao có nguy cơ có ý nghĩa cần nhập viện ICU với OR tương ứng là 3,6 (95%CI 1,8-7,0), 9,0 (95%CI 3,6-22,6), 3,0 (95%CI 1,3-7,1) và 2,5 (95%CI 1,3-4,7).
Như vậy, sự thiếu máu, sự tăng tỷ lệ bạch cầu trung tính trên tế bào lympho (>8), tăng tỷ lệ tiểu cầu trên tế bào lympho (>192) và tăng mức độ D-dimer (>0,9 mg/L) tại thời điểm nhập viện là những yếu tố dự báo cho COVID-19 nặng, cần đưa vào đơn vị chăm sóc tích cực (ICU).
3. Vai trò của các dấu ấn sinh học trong theo dõi đáp ứng điều trị COVID-19
Hầu hết dấu ấn sinh học đều có thể thay đổi khi bị COVID-19 và có thể tương quan với mức độ nghiêm trọng và khả năng sống sót, nhưng hiện chưa có dấu ấn sinh học nào được chứng minh một cách đầy đủ để có thể giúp bác sĩ lâm sàng đánh giá đáp ứng và hướng dẫn điều trị. Mặc dù một số nghiên cứu đã ghi nhận có sự liên quan giữa mức độ nặng của bệnh COVID-19 và mức độ trong huyết thanh của CRP, IL-6, IL-10, TNF-alpha, prothrombin (PT) và D-dimer, nhưng tính lợi ích lâm sàng của các dấu ấn sinh học này còn chưa rõ ràng, cho đến nay, thường chỉ giới hạn ở sự sử dụng CRP và IL-6.
Một nghiên cứu về những thay đổi của một số dấu ấn sinh học trong quá trình điều trị COVID-19 bằng abidol, lopinavir/ ritonavir và methylprednisolone đã được công bố. Sau khi điều trị, nồng độ IL-2R, IL-6, TNF-α và CRP giảm có ý nghĩa, tiếp theo là IL-8, IL-10 và PCT. Tế bào lympho T CD4+ và CD8+ tăng có ý nghĩa nhưng số lượng các tế bào lympho B và tế bào giết tự nhiên (natural killer cells) không thay đổi. Ferritin huyết thanh cũng giảm không có ý nghĩa (Samprathi M and Jayashree M, 2020 [9]).
Nồng độ D-dimer cũng được khuyến cáo có thể được sử dụng như một trong số những tiêu chuẩn phân tầng nguy cơ để quyết định chống đông máu. IL-6 đã được sử dụng để theo dõi hiệu quả điều trị bằng Tocilizumab ở những bệnh nhân COVID-19 bị bệnh phổi nặng có nồng độ IL-6 tăng (Weidmann MD, 2021 [12]).
Gần đây, Hiệp hội Quốc tế về Xét nghiệm Y học và Hóa Lâm sàng (International Federation of Clinical Chemistry and Laboratory Medicine: IFCC) khuyến cáo nên sử dụng các dấu ấn sinh học một cách thận trọng trong thực tế lâm sàng, đặc biệt là khi sử dụng các giá trị cắt. Các nghiên cứu chặt chẽ hơn nữa để tìm ra các dấu ấn sinh học đủ điều kiện sử dụng để theo dõi đáp ứng điều trị bệnh nhân nhiễm SARS-CoV-2 là cần thiết (Thompson S, 2020 [10]).
4. Các dấu ấn sinh học được sử dụng để đánh giá nguy cơ tử vong
Loomba RS và cộng sự, 2022 [6] tổng kết 10 nghiên cứu với 1.584 bệnh nhân COVID-19, trong số những bệnh nhân này, có 500 (31,5%) tử vong. Tuổi trung bình của bệnh nhân là 55,8 tuổi và 58,6% số bệnh nhân là nam. 41,4% số bệnh nhân mắc một số bệnh nền đi kèm. Tăng huyết áp là 23,1%, đái tháo đường là 11,5%, bệnh tim mạch là 6,0% và bệnh phổi mạn tính là 4,4%. Kết quả cho thấy ở bệnh nhân tử vong, các dấu ấn sinh học tăng một cách có ý nghĩa gồm số lượng bạch cầu, số lượng bạch cầu trung tính, CRP, hsCRP, procalcitonin, ferritin, D-dimer, IL-6, LDH, CK , PT, AST, ALT, bilirubin toàn phần và creatinin; các dấu ấn sinh học giảm một cách có ý nghĩa gồm số lượng tế bào lympho, số lượng tiểu cầu và albumin (Bảng 5).
Bảng 5: So sánh giá trị của các dấu ấn sinh học ở các bệnh nhân COVID-19 tử vong và sống sót (Loomba RS, 2022 [6])
|
Các dấu ấn sinh học |
Giá trị trung bình ở bệnh nhân tử vong |
Giá trị trung bình ở bệnh nhân sống sót |
Sự khác nhau trung bình (95%CI) |
P |
|
Số lượng bạch cầu (109/L) |
9,32 |
5,47 |
3,67 (2,86-4,48) |
<0,01 |
|
Số lượng BC trung tính (109/L) |
8,26 |
3,75 |
3,82 (2,19-5,46) |
<0,01 |
|
Số lượng tế bào lympho (109/L) |
0,65 |
1,07 |
-0,43 (-0,50- -0,35) |
<0,01 |
|
Số lượng tiểu cầu (109/L) |
167,30 |
202,85 |
-31,5 (-49,7- -13,2) |
<0,01 |
|
Hemoglobin (g/dL) |
12,78 |
12,77 |
-0,03 (-0,29-0,23) |
=0,82 |
|
CRP (mg/L) |
112,92 |
26,08 |
83,95 (71,3 -96,6) |
<0,01 |
|
hsCRP (mg/L) |
106,47 |
29,79 |
56,71 (13,07-100,34) |
=0,01 |
|
PCT (ng/mL) |
0,67 |
0,10 |
0,29 (0,13-0,44) |
<0,01 |
|
Tốc độ máu lắng (mm/h) |
45,75 |
49,97 |
6,77 (-0,13-13,66) |
=0,05 |
|
Ferritin (µg/L) |
1393,96 |
557,80 |
836,69 (707,1-966,3) |
>0,01 |
|
D-dimer (µg/mL) |
8,62 |
1,02 |
5,24 (2,42-8,05) |
<0,01 |
|
IL-6 (pg/mL) |
43,37 |
17,41 |
12,45 (6,50-18,39) |
<0,01 |
|
LDH (U/L) |
615,75 |
282,81 |
242,39 (169,8-314,9) |
<0,01 |
|
CK (U/L) |
214,80 |
93,74 |
63,71 (28,33-99,10) |
<0,01 |
|
CK-MB (U/L) |
18,89 |
15,14 |
4,41 (-0,33-9,15) |
=0,07 |
|
PT (s) |
13,96 |
12,48 |
1,33 (0,84-1,81) |
<0,01 |
|
PTT (s) |
40,12 |
36,61 |
0,14 (-5,06-5,34) |
=0,96 |
|
AST (U/L) |
87,90 |
32,91 |
13,31 (7,00-19,62) |
<0,01 |
|
ALT (U/L) |
52,39 |
30,45 |
4,99 (0,82-9,16) |
=0,02 |
|
Bilirubin toàn phần (mg/dL) |
0,99 |
0,73 |
0,28 (0,22-0,34) |
<0,01 |
|
Creatinin (mg/dL) |
1,05 |
0,90 |
0,13 (0,05-0,21) |
<0,01 |
|
Albumin (g/dL) |
2,96 |
3,48 |
-0,5 (-0,62- -0,38) |
<0,01 |
Ghi chú: CRP: protein phản ứng C; hsCRP (): CRP độ nhạy cao; PCT: procalcitonin; IL-6: interleukin-6 (IL-6); LDH: lactate dehydrogenase; CK: creatine kinase; CK-MB: creatine kinase MB; PT (prothrombin time): thời gian prothrombin; aPTT (activated partial thromboplastin time): thời gian thromboplastin một phần hoạt hóa; AST: aspartate aminotransferase; ALT: alanine aminotransferase.
Khalid A và cộng sự, 2021 [5] trong một nghiên cứu trên 317 ca nhập viện, thấy rằng ở bệnh nhân COVID-19 so với nhóm đối chứng khỏe mạnh, các thông số Huyết học như số lượng các tế bào lympho (lymphocytes) và tiểu cầu (platelets) giảm, trong khi số lượng bạch cầu (white blood cells), số lượng bạch cầu trung tính (neutrophil), tỷ lệ bạch cầu trung tính trên tế bào lympho (neutrophil-to-lymphocyte ratio: NLR) và tỷ lệ tiểu cầu trên tế bào lympho (platelet-to-lymphocyte ratio: PLR) tăng một cách rất rõ rệt (p<0,001). Các thông số Hóa sinh của các ca bệnh như Ferritin, D-Dimer, CRP, IL-6, LDH, ALT, AST và aPTT cũng có sự khác biệt có ý nghĩa thống kê rất rõ rệt so với giá trị tham chiếu (p<0,001). So sánh giữa các nhóm bệnh nặng và không nặng cho thấy có sự khác nhau có ý nghĩa đối với số lượng bạch cầu, số lượng bạch cầu trung tính, NLR (p<0,001) và PLR (p=0,06). So sánh các ca bệnh và đối chứng bằng các giá trị cắt tương ứng cũng thấy có sự khác biệt có ý nghĩa rất rõ rệt (p <0,001).
Sự giảm bạch cầu (lymphopenia), giảm tiểu cầu (thrombocytopenia), tăng bạch cầu trung tính (neutrophilia), tăng tế bào lympho (leukocytosis) cũng như tăng mức độ IL-6, ferritin, D-dimer, AST, LDH, procalcitonin, creatinine và CRP là các dấu ấn của các trường hợp nặng và tử vong của COVID-19. Ferritin và IL-6 là những dấu ấn sinh học quan trọng của Hội chứng bão cytokine (cytokine storm syndrome: CSS), và sự tăng mức độ của một trong hai dấu ấn này có thể được xem là dấu hiệu báo động (red flags) của tình trạng viêm hệ thống và tiên lượng xấu ở COVID-19, đặc biệt là ở người già và có bệnh nền (Melo AKG, 2021 [7]).
Gần đây, phương pháp đánh giá nguy cơ tử vong ở những bệnh nhân mắc COVID-19 nặng nhanh và đáng tin cậy bằng toán đồ (nomogram), sử dụng kỹ thuật máy học (machine learning technique), dựa trên các yếu tố nguy cơ như tuổi, số lượng tế bào bạch cầu, D-dimer, CRP, và creatinine, đã được đưa vào thử nghiệm trên thực tế lâm sàng (Rahman T, 2021 [8]).
Nói chung, vai trò của các dấu ấn Huyết học và Hóa sinh trong đánh giá mức độ nặng, theo dõi đáp ứng điều trị và tiên lượng bệnh COVID-19 có thể được tóm tắt ở Bảng 6.
Bảng 6. Vai trò của các dấu ấn Huyết học và Hóa sinh trong đánh giá mức độ nặng, theo dõi đáp ứng điều trị và tiên lượng bệnh COVID-19 (Samprathi M and Jayashree M, 2020 [9]).
|
Vai trò |
Các dấu ấn sinh học |
|
Chẩn đoán |
Giảm bạch cầu; giảm lympho; tỷ lệ NLR cao; ↑LDH; ↑AST |
|
Đánh giá mức độ nặng của bệnh |
Giảm bạch cầu; Các tập hợp con của các tế bào lympho: ↓ CD4+, CD8+, B, tế bào giết tự nhiên (NK); ↑ tế bào plasma; ↑ NLR và ↓ LCR; ↑ Tỷ lệ IL-2R/Tế bào lympho; ↑ IL-6; ↑ CRP, PCT; ↑ Ferritin; ↑ LDH; ↑ D-dimers; ↑ Các dấu ấn sinh học đặc hiệu tim: CK-MB, cTnT, Mb, NT-proBNP |
|
Theo dõi đáp ứng điều trị |
↓ CRP; ↓ IL-6, IL-10, TNF-alpha, IL-2R |
|
Tiên lượng
|
IL-6; Ferritin; LDH; CRP, PCT; số lượng tế bào lympho; NLR; LCR; số lượng tiểu cầu; các dấu ấn sinh học đặc hiệu tim: CK-MB, cTnT, Mb, NT-proBNP |
|
Hội chứng viêm đa hệ thống ở trẻ em (MIS-C) |
↓ Tiểu cầu; ↑ CRP, ESR, PCT; ↓ Albumin; ↑ các dấu ấn sinh học đặc hiệu tim: CK-MB, CTnT, NT-proBNP; ↑ IL-6, IL-10, TNF-alpha; ↑ D-dimers |
Ghi chú: ALT: alanin transaminase; AST: aspartate transaminase; CK: creatine kinase; CRP (C-reactive protein): protein phản ứng C; cTnT (cardiac troponin-T): troponin-T tim; ESR: tốc độ lắng hồng cầu; IL-6: interleukin-6; LCR (các tế bào lympho to CRP ratio): tỷ lệ tế bào lympho trên CRP; LDH: lactate dehydrogenase; NLR (neutrophil to các tế bào lympho ratio): tỷ lệ bạch cầu trung tính trên tế bào lympho; NT-proBNP (N terminal pro brain natriuretic peptide): peptide bài niệu natri lợi niệu pro đầu tận N; PCT: procalcitonin; SAA (serum amyloid A): amyloid A huyết thanh; TNF-alpha (alpha, tumor necrosis factor-alpha): yếu tố hoại tử khối u-alpha; WBC (white blood cell): Bạch cầu; MIS-C (Multisystem Inflammatory Syndrome in Children): Hội chứng viêm đa hệ thống ở trẻ em.
5. Các dấu ấn sinh học sử dụng ở trẻ em bị COVID-19
Điều may mắn là trẻ em bị COVID-19 hầu hết không có triệu chứng hoặc bị bệnh nhẹ hơn nhiều so với người lớn. Trong một phân tích tổng hợp ở trẻ em bị nhiễm COVID-19, 20% không có triệu chứng; 33% bị bệnh nhẹ và 51% là bệnh vừa. Số trẻ em bị COVID-19 phải nhập viện chỉ chiếm 0,1% đến 1,5% tổng số ca phải nhập viện và số trẻ em bị tử vong chỉ chiếm 0,00% đến 0,01% tổng số ca tử vong do COVID-19.
Đối với các bệnh nhi bị COVID-19 phải nhập viện, trong một nghiên cứu trên 633 bệnh nhi gồm 83 (13,1%) bệnh nhi nhập viện và 550 (86,9%) bệnh nhi được theo dõi tự cách ly tại nhà, Alkan G và cộng sự, 2021 [1] thấy ở nhóm bệnh nhi phải nhập viện có sự tăng bạch cầu (leukocytosis), tăng bạch cầu đa nhân trung tính (neutrophilia), tăng tiểu cầu (thrombocytosis), tăng CRP, tăng procalcitonin và D-dimer một cách có ý nghĩa rõ rệt (Bảng 7).
Bảng 7. So sánh một số thông số Huyết học và Hóa sinh ở trẻ em COVID-19 điều trị ngoại trú và nội trú (Alkan G, 2021 [1])
|
Các thông số, n (%) |
Bệnh nhi nhập viện 83 (13,1) |
Bệnh nhi nhập viện 550 (86,9) |
Tổng số 633 (100) |
Giá trị P |
|
Tăng bạch cầu |
7 (8,5) |
5 (0,9) |
12 (1,8) |
<0,001 |
|
Giảm bạch cầu |
17 (20,5) |
105 (19,1) |
122 (19,2) |
0,765 |
|
Tăng bạch cầu trung tính |
8 (9,6) |
9 (1,6) |
17 (2,6) |
<0,001 |
|
Giảm bạch cầu trung tính |
8 (9,6) |
40 (7,3) |
48 (7,6) |
0,448 |
|
Tăng các tế bào lympho |
1 (1,2) |
1 (0,2) |
2 (0,3) |
0,122 |
|
Giảm tế bào lympho |
24 (28,9) |
204 (37,1) |
228 (36) |
0,320 |
|
Tăng tiểu cầu |
15 (18,1) |
41 (7,5) |
56 (8,8) |
0,001 |
|
Giảm tiểu cầu |
3 (3,6) |
12 (2,2) |
15 (2,4) |
0,424 |
|
Thiếu máu |
6 (7,2) |
27 (4,9) |
33/633 (5,2) |
0,375 |
|
CRP (>8 mg/L) |
30/83 (36,1) |
101/549 (18,4) |
131/632 (20,7) |
<0,001 |
|
Procalcitonin (>0,5 µg/L) |
10/80 (12,5) |
5/540 (0,9) |
15/620 (2,4) |
<0,001 |
|
D-dimer (>500 ng/mL) |
17/50 (34) |
67/420 (16) |
84/470 (17,9) |
0,002 |
Nói chung, các bất thường về xét nghiệm ở trẻ em bị COVID-19 là không phổ biến và chủ yếu chỉ giới hạn ở trẻ bị bệnh nặng và hội chứng viêm đa hệ thống ở trẻ em (Multisystem Inflammatory Syndrome in Children: MIS-C).
Đối với tất cả trẻ em nghi ngờ bị hội chứng viêm đa hệ thống ở trẻ em (MIS-C), cần thực hiện các xét nghiệm theo khuyến cáo của WHO, đó là: (1) các dấu hiệu viêm gồm máu lắng (ESR), protein phản ứng C, hoặc procalcitonin và ferritin; (2) các dấu ấn sinh học tim gồm TnT/ NT-proBNP, và (3) các dấu ấn của rối loạn đông máu gồm PT, aPTT và D-dimers.
Các bệnh nhi bị bệnh hô hấp nặng và bị hội chứng viêm đa hệ thống ở trẻ em (MIS-C) thường có mức độ CRP, procalcitonin hoặc troponin cao hơn, trong khi số lượng tiểu cầu và mức độ natri huyết thanh thấp hơn so một cách rõ rệt so với những trẻ bị bệnh nhẹ (Samprathi M and Jayashree M, 2020 [9]).
Tóm lại, các dấu ấn sinh học để chẩn đoán COVID-19 có thể gồm rRT-PCR là xét nghiệm tiêu chuẩn để chẩn đoán, trong khi xét nghiệm kháng nguyên nhanh là xét nghiệm miễn dịch để phát hiện sự hiện diện của một kháng nguyên đặc hiệu của virus và các xét nghiệm kháng thể (huyết thanh học) là các xét nghiệm được sử dụng để phát hiện sự nhiễm SARS-CoV-2 trước đó. Các dấu ấn sinh học để theo dõi đáp ứng điều trị ở bệnh nhân COVID-19 đang được tiếp tục đánh giá có thể gồm CRP, IL-6, PT và D-dimer. Các dấu ấn sinh học để dự đoán bệnh nặng ở bệnh nhân COVID-19 có thể gồm sự thiếu máu, sự tăng của tỷ lệ bạch cầu trung tính/ tế bào lympho, tỷ lệ tiểu cầu/ tế bào lympho và mức độ D-dimer tại thời điểm nhập viện có thể giúp dự báo bệnh nặng cần nhập viện ICU. Các dấu ấn sinh học để dự đoán tử vong ở bệnh nhân COVID-19 có thể gồm sự tăng của số lượng bạch cầu, số lượng bạch cầu trung tính, CRP, hsCRP, procalcitonin, ferritin, D-dimer, IL-6, PT, LDH, CK, AST, ALT, bilirubin toàn phần và creatinine và sự giảm của số lượng tế bào lympho, số lượng tiểu cầu và albumin. So với bệnh nhi COVID-19 ngoại trú, bệnh nhi nội trú có số lượng bạch cầu, tế bào lympho và tiểu cầu, CRP, procalcitonin, D-dimer và tỷ lệ lymphocyte trên monocyte cao hơn một cách có ý nghĩa. Trẻ bị bệnh hô hấp nặng và hội chứng viêm đa hệ thống ở trẻ em (MIS-C) có mức độ CRP, procalcitonin hoặc troponin cao hơn, trong khi số lượng tiểu cầu hoặc mức độ Natri huyết thanh thấp hơn một cách có ý nghĩa so với những trẻ bị bệnh nhẹ.
Tài liệu tham khảo
1. Alkan G, Sert A, Emiroglu M, Oz SKT, Vatansev H. Evaluation of hematological parameters and inflammatory markers in children with COVID-19. Ir J Med Sci 2021 Sep 16: 1-9.
2. Bivona G, Agnello L, and Ciaccio M, Biomarkers for Prognosis and Treatment Response in COVID-19 Patients. Ann Lab Med 2021 Nov 1; 41(6): 540-548.
3. Bohn MK, Lippi G, Horvath A, et al. Molecular, serological, and biochemical diagnosis and monitoring of COVID-19: IFCC taskforce evaluation of the latest evidence. Clin Chem Lab Med 2020 Jun 25; 58(7): 1037-1052.
4. Hashem MK, Khedr EM, Daef E, et al. Prognostic biomarkers in COVID-19 infection: value of anemia, neutrophil-to-các tế bào lympho ratio, platelet-to-các tế bào lympho ratio, and D-dimer. Egypt J Bronchol 2021; 15(1): 29.
5. Khalid A, Jaffar MA, Khan T, et al. Hematological and biochemical parameters as diagnostic and prognostic markers in SARS-COV-2 infected patients of Pakistan: a retrospective comparative analysis. Hematology 2021 Dec; 26(1): 529-542.
6. Loomba RS, Villarreal EG, Farias JS, et al. Serum biomarkers for prediction of mortality in patients with COVID-19. Ann Clin Biochem 2022 Jan; 59(1): 15-22.
7. Melo AKG, Milby KM, Caparroz ALMA, et al. Biomarkers of cytokine storm as red flags for severe and fatal COVID-19 cases: A living systematic review and meta-analysis. PLoS One 2021; 16(6): e0253894.
8. Rahman T, Al-Ishaq FA, Al-Mohannadi FS, et al. Mortality Prediction Utilizing Blood Biomarkers to Predict the Severity of COVID-19 Using Machine Learning Technique. Diagnostics (Basel) 2021 Sep; 11(9): 1582.
9. Samprathi M and Jayashree M. Biomarkers in COVID-19: An Up-To-Date Review. Front Pediatr 2020; 8: 607647.
10. Thompson S, Bohn MK, Mancini N, et al. IFCC Interim Guidelines on Biochemical/Hematological Monitoring of COVID-19 Patients. Clin Chem Lab Med 2020 Oct 7; 58(12): 2009-2016.
11. Ulinici M, Covantev S, Wingfield-Digby J, et al. Screening, Diagnostic and Prognostic Tests for COVID-19: A Comprehensive Review. Life (Basel) 2021 Jun; 11(6): 561.
12. Weidmann MD, Ofori K and Rai AJ. Laboratory Biomarkers in the Management of Patients With COVID-19. Am J Clin Pathol 2021 Feb 11; 155(3): 333-342.
Bình luận ()
Lựa chọn dịch vụ
Quý khách hàng vui lòng lựa chọn dịch vụ y tế theo nhu cầu!